Lewis struktur av ClO3 – ion er trukket trinn for trinn i denne opplæringen. Totalt valence elektroner til oksygen og klor-atomer og negativ ladning er vurdert å trekke ClO3 – lewis-struktur. Når vi trakk lewis struktur, samlet kostnad av ion bør være -1.
Lewis Struktur av nitritt ion
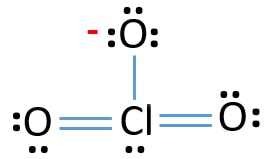
Nå, vi kommer til å lære, hvordan å trekke dette lewis struktur av ClO3 – ion-trinn for trinn.,
Trinnene for å trekke ClO3 – lewis-struktur
Følgende trinn er nødvendige for å tegne ClO3 – lewis-struktur og de er forklart i detalj i denne opplæringen.
- Finne totalt antall elektroner av valance skall av klor og oksygen atomer og inkludert kostnad av anion
- Totalt elektroner par i valence skjell
- Bestemme center atom fra klor og oksygen atom
- Sette enslig par på atomer
- Stabilitet av lewis-struktur – Sjekk stabilitet og minimere kostnader på atomer ved å konvertere enslig par til obligasjoner for å få den beste strukturen.,
Tegning riktig lewis struktur er viktig å trekke resonans strukturer av ClO3-.
Totalt antall elektroner av valance skall av klor og oksygen atomer og kostnad av anion
Det er en klor-atomet og tre oksygen atomer i chlorate ion. Det er også -1 avgift på ClO3 – ion.
Klor og oksygen er plassert på 7 og 6 grupper, henholdsvis i den periodiske tabell. Så klor har sju elektroner i sitt valence shell. I oksygen atom, det er seks elektroner i sitt valence shell.,hlorine atomer = 7*1 = 7
Det er tre oksygen atomer i ClO3 – Derfor
- Totalt valence elektroner gitt av oksygen atomer = 6 *3 = 18
på Grunn av -1 kostnad, annen elektroner er lagt
- på Grunn av -1 lade, mottatt elektroner til valence elektroner= 1
- Totalt valence elektroner = 7 + 18 + 1 = 26
Totalt valence elektroner par
Totale valance elektroner par = σ obligasjoner + π obligasjoner + enslig par i valence skjell
Totale electron parene bestemmes ved å dividere antall totalt valence av to elektroner., For, ClO3 – det er 26 valence elektroner, så totalt par av elektroner er 13.
Center atom av ClO3 – ion
Å være sentrum atom, evnen til å ha større valance er viktig. Klor kan vise valence 7. Men, oksygen er maksimal valence er 2. Derfor klor har større sjanse til å være sentrum atom (Se figur). Så, nå kan vi bygge en skisse av ClO3 – ion.
Skisse av ClO3 – ion
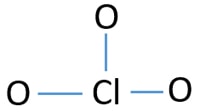
Enslig par på atomer
- Det er allerede tre Cl-O obligasjoner i skissen., Derfor er det bare ti valence elektroner par som er igjen å trekke resten av ion.
- Neste trinn er, markerer de ti valence elektroner par på utsiden atomer (oksygen atomer) som enslig par. Ett oksygen atom vil ta tre enslig par følge oktale regel (oksygen atomer kan ikke holde mer enn åtte elektroner i sitt valence skjell). Derfor, ni par elektroner er merket på tre oksygen atomer. Nå, ett par elektroner (10-9) er igjen.
- Så, igjen electron par er merket på klor-atomet.,
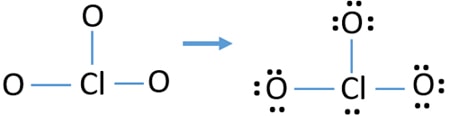
Se stabilitet trukket struktur av ClO3 – ion og redusere kostnader på atomer ved å konvertere enslig par til obligasjoner
Sjekk priser på atomer og merke dem som nedenfor. Kostnader er viktig for å bestemme det beste lewis struktur av ion.

Den tegnede struktur for ClO3 – er ikke en stabil struktur fordi oksygen atomer og kloratomer har kostnader. Også, når ansvaret for et atom er store, at strukturen blir mer ustabil. Når et molekyl eller ion har så mange avgifter på atomer, at struktur er ikke stabil.,
Nå, vi bør prøve å minimere kostnader ved å konvertere enslig par eller par som finnes på oksygen atomer til obligasjoner. Så vi konvertere en enslig par av ett oksygen atom som en Cl-O bond som i følgende figur.
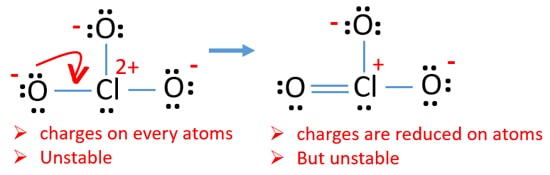
Nå er det et dobbelt bånd mellom klor og ett oksygen atom. Det er også to enkle obligasjoner (Cl-O) med klor atom og to andre oksygen atomer.
Men, det er fortsatt avgifter på atomer. Hvis det er mulig, bør vi redusere kostnader videre. En annen enslig par på annen oksygen atom overføres som en Cl-O bond.,
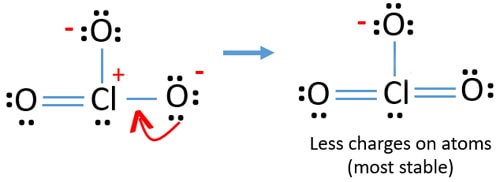
Nå, det er tolv elektroner rundt klor-atomet. Dette er akseptabelt fordi klor kan holde mer enn åtte elektroner klor har beholdningen av 3d-baner.
I ny struktur, kostnader av atomer er redusert videre. Nå er det ikke noen kostnad på to oksygen atomer. Også ansvaret for klor-atomet er redusert til null. Nå kan du forstå denne strukturen av ClO3 – er mer stabil enn tidligere struktur på grunn av lavere kostnader på atomer.,
ClO3 – Lewis-struktur

Spørsmål
Spør din kjemi spørsmål og finne svar
Hva er formen rundt klor-atomet i ClO3 – ion?
Det er tre σ obligasjoner og ett enslig par rundt klor-atomet i lewis struktur av ClO3 – ion. Derfor form av ion er trigonal pyramidal.
Hvor mange ladninger i atomer av chlorate ion-lewis-strukturen?
Bare ett oksygen atom har en -1 kostnad. Alle andre atomer ikke har avgifter. Derfor samlet kostnad på chlorate ion er -1.,
clo3 lewis struktur
Det er ingen molekyl eller ion som ClO3. The riktige formelen for chlorate ion er ClO3-.