struktura Lewisa ClO3-jonu jest rysowana krok po kroku w tym tutorialu. Całkowite elektrony walencyjne atomów tlenu i chloru oraz ładunek ujemny są uważane za wzór struktury ClO3-Lewisa. Kiedy narysujemy strukturę Lewisa, całkowity ładunek jonu powinien wynosić -1.
struktura Lewisa jonów azotynowych
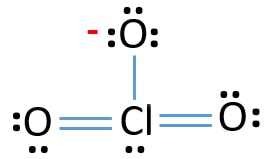
teraz nauczymy się, jak narysować tę strukturę Lewisa jonów Klo3 krok po kroku.,
etapy rysowania struktury ClO3 – lewis
następujące kroki są wymagane do narysowania struktury ClO3 – lewis i są szczegółowo wyjaśnione w tym samouczku.
- Znajdź całkowitą liczbę elektronów powłokach walencyjnych atomów chloru i tlenu i w tym ładunek anionu
- całkowite pary elektronów w powłokach walencyjnych
- Określ ATOM centrum z atomu chloru i tlenu
- umieść samotne pary na atomach
- stabilność struktury Lewisa – Sprawdź stabilność i zminimalizuj ładunki na atomach, przekształcając samotne pary w wiązania, aby uzyskać najlepszą strukturę.,
rysowanie poprawnej struktury Lewisa jest ważne przy rysowaniu struktur rezonansowych ClO3-.
całkowita liczba elektronów powłok walankowych atomów chloru i tlenu oraz ładunku anionu
w Jonie chloranowym znajduje się jeden atom chloru i trzy atomy tlenu. Ponadto na ClO3 – ionie znajduje się ładunek A -1.
chlor i tlen znajdują się odpowiednio w 7 i 6 grupach układu okresowego. Więc chlor ma siedem elektronów w swojej powłoce walencyjnej. W atomie tlenu w jego powłoce walencyjnej znajduje się sześć elektronów.,hlorine Atomy = 7*1 = 7
istnieją trzy atomy tlenu w ClO3- , dlatego
- całkowite elektrony walencyjne podane przez atomy tlenu = 6 *3 = 18
ze względu na ładunek -1 dodaje się kolejne elektrony
- ze względu na ładunek -1, otrzymane elektrony do elektronów walencyjnych= 1
- razem elektrony walencyjne = 7 + 18 + 1 = 26
pary elektronów walencyjnych ogółem
pary elektronów walencyjnych ogółem = σ wiązania + π wiązania + samotne pary w powłokach walencyjnych
pary elektronów ogółem określa się przez podzielenie liczby elektronów walencyjnych ogółem przez dwa., Dla ClO3-jest 26 elektronów walencyjnych, więc razem par elektronów jest 13.
Atom Centralny Klo3 – jonu
aby być atomem centralnym, ważna jest zdolność posiadania większej walancji. Chlor może pokazać Walencję 7. Ale maksymalna wartość tlenu wynosi 2. W związku z tym chlor ma większą szansę być atomem centrum (patrz rysunek). Więc teraz możemy zbudować szkic ClO3-Iona.
Sketch of ClO3 – ion
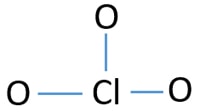
samotne pary na atomach
- w szkicu są już trzy wiązania Cl-O., W związku z tym pozostało tylko dziesięć par elektronów walencyjnych, aby narysować resztę jonu.
- następnym krokiem jest oznaczenie tych dziesięciu par elektronów walencyjnych na zewnętrznych atomach (atomach tlenu) jako samotnych par. Jeden atom tlenu zajmie trzy samotne pary zgodnie z zasadą ósemkową (atomy tlenu nie mogą utrzymać więcej niż ośmiu elektronów w swoich powłokach walencyjnych). W związku z tym na trzech atomach tlenu zaznaczonych jest dziewięć par elektronów. Obecnie pozostaje jedna para elektronów (10-9).
- następnie na atomie chloru zaznacza się pozostałą parę elektronową.,
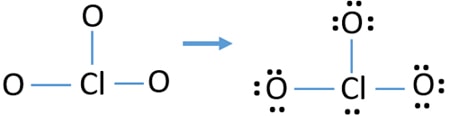
Sprawdź stabilność rysowanej struktury ClO3 – jonu i zmniejsz ładunki na atomach, przekształcając pojedyncze pary w wiązania
Sprawdź ładunki na atomach i oznacz je jak poniżej. Ładunki są ważne, aby decydować o najlepszej strukturze jonu.

rysowana struktura ClO3 – nie jest strukturą stabilną, ponieważ atomy tlenu i chloru mają ładunki. Ponadto, gdy ładunek atomu jest duży, struktura ta staje się bardziej niestabilna. Kiedy cząsteczka lub jon ma tak wiele ładunków na atomach, struktura ta nie jest stabilna.,
teraz powinniśmy starać się minimalizować ładunki, zamieniając samotne pary lub pary występujące na atomach tlenu na wiązania. Konwertujemy więc jedną samotną parę jednego atomu tlenu jako Wiązanie Cl-O, jak na poniższym rysunku.
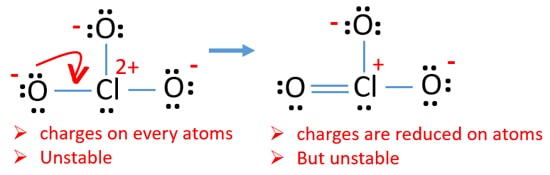
teraz istnieje wiązanie podwójne między chlorem a jednym atomem tlenu. Istnieją również dwa pojedyncze wiązania (Cl-O) z atomem chloru i innymi dwoma atomami tlenu.
ale nadal są ładunki na Atomy. Jeśli to możliwe, powinniśmy ponadto obniżyć opłaty. Inna para na innym atomie tlenu jest przenoszona jako Wiązanie Cl-O.,
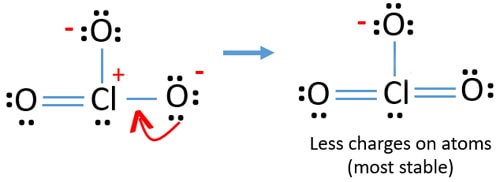
teraz wokół atomu chloru jest dwanaście elektronów. Jest to dopuszczalne, ponieważ chlor może zatrzymać więcej niż osiem elektronów chlor ma niewypełnione orbity 3d.
w nowej strukturze ładunki atomów są dodatkowo zmniejszane. Teraz nie ma żadnego ładunku na dwóch atomach tlenu. Ponadto ładunek atomu chloru jest zredukowany do zera. Teraz rozumiesz, że struktura ClO3 – jest bardziej stabilna niż poprzednia struktura z powodu mniejszej ilości ładunków na atomach.,
struktura ClO3 – Lewisa

Pytania
zadaj pytania chemiczne i znajdź odpowiedzi
jaki jest kształt wokół atomu chloru w jonach ClO3?
istnieją trzy wiązania σ i jedna para wokół atomu chloru w strukturze Lewisa klo3 – jonu. W związku z tym kształt jonu jest trygonalny piramidalny.
ile ładunków w atomach struktury jonów chloranowych?
tylko jeden atom tlenu ma ładunek a -1. Wszystkie inne atomy nie mają ładunków. W związku z tym całkowity ładunek jonu chloranowego wynosi -1.,
clo3 struktura Lewisa
nie ma cząsteczki ani jonu jako ClO3. Prawidłowy wzór jonu chloranowego to ClO3-.