Hvordan virker en blanding av en svak syre og dens kobling base hjelpe buffer en løsning mot pH-endringer?
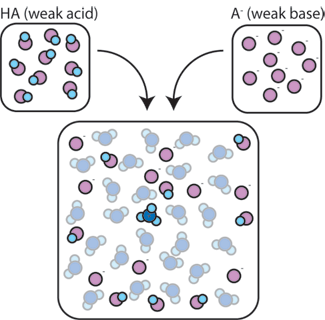
Hvis vi blander en svak syre (HA) med sin kobling base – (A-), både syre og base komponenter være til stede i løsningen. Dette er fordi de ikke gjennomgår noen reaksjoner som vesentlig endrer sin konsentrasjoner. Syre og konjugat base kan reagere med hverandre, HA + A- → A- + HA, men når de gjør det, de bare handel steder og konsentrasjoner og endres ikke. I tillegg, HA og bare sjelden reagerer med vann., Ved definisjon, en svak syre er en som bare sjelden dissosierer i vann (som er, bare sjelden vil syre miste sin proton H+ vann). Likeledes, siden konjugat base-En – er en svak base, er det sjelden stjeler en proton H+ fra vann.
Så, svak syre og en svak base forblir i løsning med høye konsentrasjoner siden de bare sjelden reagerer med vann. De er imidlertid svært sannsynlig til å reagere med noen ekstra sterk base eller sterk syre.,
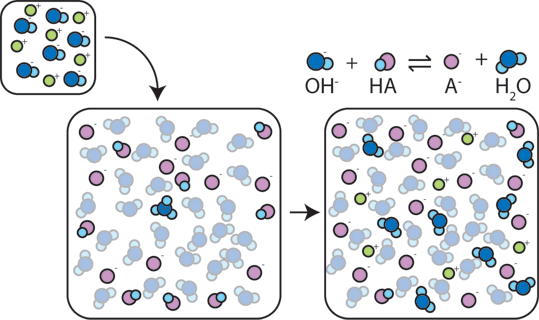
Hvis en sterk base er lagt til en buffer, svak syre vil gi opp sin H+ for å forvandle base (OH-) i vann (H2O) og konjugat base: HA + OH- → A- + H2O. Siden lagt OH – er fortært av denne reaksjonen, pH, endres bare litt.
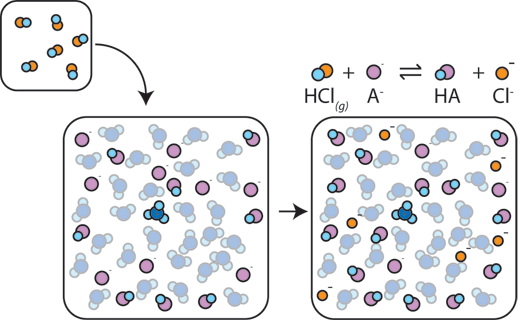
Hvis en sterk syre som er lagt til en buffer, den svake basen vil reagere med H+ fra sterk syre til å danne svak syre HA: H+ + A- → HA. H+ blir absorbert av En – i stedet for å reagere med vann og danner H3O+ (H+), slik at pH-endringer bare litt.,
Se neste side for en veileder som leder deg gjennom de beregninger som er involvert i å lage en buffer.