ce este volatilitatea ?se spune că o substanță este volatilă dacă fierbe la o temperatură scăzută, trecând de la lichid la faza gazoasă.substanțele care sunt gaze la temperatura camerei sunt extrem de volatile: au o volatilitate ridicată. Ele pot fi văzute doar ca lichide atunci când sunt expuse la temperaturi scăzute sau presiuni ridicate.tabelul de mai jos prezintă unele substanțe aranjate în ordinea descrescătoare a punctului de fierbere și creșterea volatilității., În tabel, borul este cel mai puțin volatil, iar hidrogenul este substanța cea mai volatilă.,
CH3(CH2)7OH
1-octanol
195
H2O
water
100
CH3OH
methanol
65
(CH3)2CO
acetone
56
CH4
methane
-161
H2
hydrogen
-253

Volatility and Vapor Pressure

At the molecular level, particles in liquids have a range of kinetic energies.,Cele mai energice particule au suficientă energie pentru a scăpa din lichid și a intra în faza gazoasă. Vedem acest lucru ca evaporare.
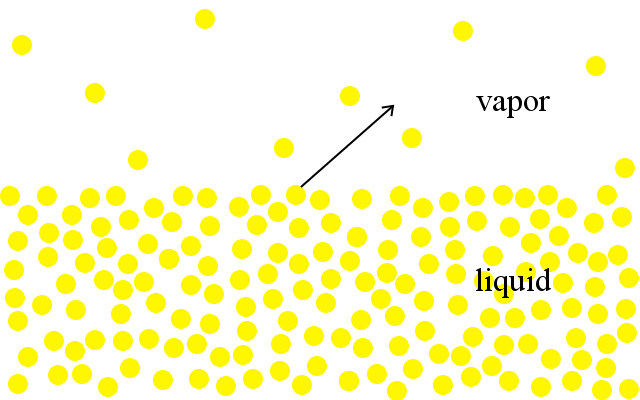
un lichid se fierbe atunci când presiunea particulelor sale care intră în faza gazoasă crește la egal cu presiunea atmosferică din jur.cu cât un lichid este mai aproape de punctul său de fierbere, cu atât este mai mare presiunea vaporilor.Lichidele cu puncte de fierbere scăzute au presiuni de vapori mai mari la orice temperatură dată decât lichidele cu puncte de fierbere ridicate.prin urmare, de exemplu, acetona cu un punct de fierbere de 56 °C are o presiune de vapori mai mare decât apa.,La temperatura camerei, acetona va intra în faza de vapori într-o măsură mai mare decât apa.Aceasta este o caracteristică a lichidelor volatile.