todos os anos, são produzidas cerca de 20 milhões de toneladas de nitrato de amónio a nível mundial. É até agora o fertilizante mais potente, econômico e conveniente do mercado, apoiando os agricultores na alimentação de bilhões. No entanto, a recente explosão catastrófica em Beirute é um lembrete dos perigos associados ao armazenamento inadequado e transporte deste produto químico comum., Como podemos aproveitar o poder do nitrato de amónio, assegurando simultaneamente que tragédias como Beirute sejam evitadas no futuro?o desastre de Beirute em 4 de agosto de 2020, uma grande quantidade de nitrato de amônio em um hangar de armazenamento no porto de Beirute explodiu, causando mais de 300 mortes e 6.000 feridos, bem como enormes danos materiais, deixando cerca de 300.000 pessoas desabrigadas., A explosão catastrófica em Beirute foi um dos poucos acidentes em grande escala causados pelo nitrato de amônio, comparável apenas a explosões na cidade do Texas, Estados Unidos (1947); Toulouse, França (2001); e Tianjin, China (2015).
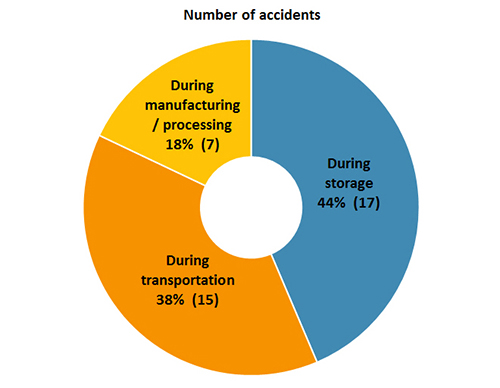
desde o início do século XX, tem havido cerca de 40 grandes acidentes, com mais de metade deles ocorrendo nos últimos 20 anos. Onze destes acidentes envolveram mais de 1 000 toneladas de nitrato de amónio ou causaram mais de 30 mortes (Figura 1). Mais de 80% destes acidentes ocorreram durante o armazenamento ou transporte de nitrato de amónio (Figura 2)., A análise destes acidentes mostra que as explosões de nitrato de amónio são quase sempre precedidas por incêndios ou outras fontes de ignição.
para mais informações sobre as propriedades químicas do nitrato de amónio, seus perigos e regras de segurança baixar este relatório CAS aprofundado.o nitrato de amónio pode ser domado?o que pode ser feito para garantir que tragédias como Beirute sejam evitadas no futuro? A chave para impulsionar a inovação futura neste espaço é compreender a estrutura molecular e as reações que causam estas poderosas explosões., O nitrato de amônio é feito por reação de amônia com ácido nítrico em água, seguido por uma cuidadosa evaporação da água.
![]()
a Amônia é mais frequentemente preparado a partir do nitrogênio atmosférico, enquanto que o ácido nítrico é preparado a partir da combustão da amônia, e portanto, o nitrato de amônio é mais convenientemente fabricado onde a amônia é feita. A formação de nitrato de amônio gera quantidades significativas de calor, sendo feito em solução aquosa para dissipar melhor esse calor., A água deve então ser removida da solução para produzir nitrato de amónio sólido, na maioria das vezes por evaporação. Embora o nitrato de amónio seja estável às temperaturas habituais da sua fabricação e purificação, os aditivos são frequentemente utilizados para reduzir os perigos. Por exemplo, compostos de potássio como nitrogênio-potássio e nitrogênio-fósforo-potássio têm sido usados para aumentar a estabilidade do nitrato de amônio para a transição de fase e diminuir a sua sensibilidade à explosão., Os nitratos de cálcio e de magnésio foram também adicionados ao nitrato de amónio em pequenas quantidades para melhorar a sua estabilidade física, mas as misturas absorvem mais facilmente a água da atmosfera. O nitrato de amónio cálcico (CAN), Preparado a partir de nitrato de amónio e carbonato de cálcio, é utilizado em alguns casos como uma alternativa ao nitrato de amónio. Sulfato de alumínio também tem sido usado como um aditivo de secagem para nitrato de amônio. Embora estas alternativas tenham ajudado, é importante notar que impurezas não intencionais no processo de fabrico podem reduzir a sua estabilidade ou facilitar a explosão.,uma análise aprofundada da recolha de conteúdos CAS revela algumas áreas-chave que começaram a emergir na paisagem da propriedade intelectual, delineando esforços para prevenir explosões acidentais ou mau uso. Estes incluem avanços em torno de misturas, revestimentos, formulações de libertação lenta, controle de tamanho de partículas, e abordagens de higroscopicidade que minimizam o potencial de uso indevido e aumentar a estabilidade para um armazenamento mais seguro., Por exemplo, foi inventado um revestimento para um fertilizante que previne a infiltração de hidrocarbonetos, como o fuelóleo, nos poros do fertilizante, reduzindo assim a sua eficácia como oxidante (WO2003106377). Alternativamente, abordagens higroscópicas também foram exploradas pela adição de um ingrediente chave, como um sal duplo de ureia que forma um fertilizante estável com nitrato de amônio (US20150218058)., Assim, surgiram algumas alternativas que fornecem aos usuários opções seguras e rentáveis, mas ainda há benefícios significativos tanto em segurança quanto em teor de nitrogênio, então mais inovação ainda é necessária. embora o nitrato de amónio seja um importante fertilizante devido ao seu elevado teor de azoto, os seus perigos explosivos limitam a sua aplicação, tendo mesmo sido proibido em algumas áreas., Reduzir a concentração de nitrato de amónio, encontrar compostos alternativos e desenvolver formas mais seguras são estratégias que podem ajudar a aumentar a segurança dos fertilizantes azotados. A tabela 1 lista os fertilizantes azotados alternativos que surgiram como opções mais seguras que poderiam fornecer substitutos ao nitrato de amônio. Infelizmente, a alternativa com o maior teor de nitrogênio é amônia anidra, que é um gás tóxico à temperatura ambiente., Outras alternativas com elevado teor de azoto, tais como soluções de hidróxido de amónio e ureia, são atraentes devido ao seu baixo custo e eficácia; no entanto, são voláteis. Foram desenvolvidas formulações de libertação lenta de ureia, bem como lenhinas e hidrogels modificados, para superar este Desafio.Tabela 1., List of alternative nitrogenous fertilizers
|
Fertilizer |
Comment |
|
|---|---|---|
|
Anhydrous ammonia |
Pressurized gas, Risk Management Plan (RMP)-regulated substance with a threshold of 10,000 lbs, regulated as Dangerous Goods for transportation.,div id=”8648a5f2f4″> Sodium nitrate |
Stable |
|
Calcium cyanamide |
Contains calcium |
|
|
Calcium nitrate |
Contains calcium |
Handling ammonium nitrate safely
Previous disasters have heightened public awareness of the explosive nature of ammonium nitrate, and the consequences of its unsafe storage and use., Em resposta, muitos regulamentos, regras e orientações para o nitrato de amónio, especialmente no que diz respeito ao seu armazenamento e manuseamento, surgiram em diferentes áreas para melhorar a segurança. Os principais regulamentos dos EUA para o nitrato de amônio são “OSHA 29 CFR 1910.109(i) – armazenamento de nitrato de amônio”, e o Memorando de “Guidance on the Ammonium Nitrate Storage Requirements in 29 CFR 1910.109(i)” publicado em 2014 após a Adair Grain Inc., DBA West Fertilizer Company explosion in 2013., Notável, no entanto, a aplicação diligente das regras e regulamentos de segurança é a chave para evitar futuros acidentes, como o desastre de Beirute., pode ser resumido como se segue:
(Figura 3):
- Ventilação: capaz de ventilação adequada em caso de incêndio
- Isolamento de combustão: não inflamável e resistente a materiais são necessários
- controle de Temperatura: a temperatura de armazenamento deve ser inferior a 130℉
- Volume: limites de armazenamento deve ser menor do que 2270 toneladas
- proteção/prevenção de Incêndios: rigoroso fogo proteções são necessárias
- prevenção de combustíveis contaminantes: a divisão de armazenamento de outros produtos
apesar das preocupações de segurança, o nitrato de amónio continua a ser um importante fertilizante em todo o mundo, uma vez que é eficaz, barato e fácil de fabricar. No entanto, como mais uma vez foi salientado pelo incidente de Beirute, a susceptibilidade do nitrato de amónio a incêndios e explosões devido a más práticas de armazenamento ou contaminação apresentam riscos significativos., Regulamentos inconsistentes e uma falta de consciência sustentada sobre como lidar e armazenar com segurança o nitrato de amônio dentro da cadeia de suprimentos global são desafios fundamentais que devem ser superados através da educação e Defesa para evitar outra tragédia global. veja como os cientistas estão a tornar o nitrato de amónio mais seguro no nosso mais recente Livro Branco lições aprendidas com o nitrato de amónio.