1Introduction
przewlekła aktywna infekcja wirusem Epsteina-Barr (CAEBV) to termin kliniczny definiowany początkowo przez firmę Straus jako choroba związana z przewlekłą lub przewlekłą infekcją EBV., Sugerowane kryteria diagnozowania ciężkiej przewlekłej infekcji EBV obejmują: 1) ciężką chorobę >trwającą 6 miesięcy, która rozpoczęła się jako pierwotna infekcja EBV i jest związana z rażąco nieprawidłowymi mianami przeciwciał EBV ; (2) zwiększoną ilością DNA EBV lub rażąco nieprawidłowym poziomem przeciwciał EBV, na przykład wykrywaniem DNA EBV w tkankach lub krwi obwodowej przez hybrydyzację Southern blot; kodowane przez EBV małe komórki RNA-1-Dodatnie w dotkniętych tkankach lub krwi obwodowej, >102.,5 kopii DNA EBV / µg DNA komórek jednojądrzastych krwi obwodowej; oraz rażąco nieprawidłowe poziomy przeciwciał EBV (miana IgG anty-VCA ≥5120 lub miana IgG anty-EA ≥640), oraz (3) Brak dowodów na wcześniejsze nieprawidłowości immunologiczne lub inne niedawne zakażenie, które mogłyby wyjaśnić obserwowany stan.,4
na podstawie zgromadzonych danych CAEBV typu limfocytów T lub NK został niedawno zdefiniowany jako ogólnoustrojowe, poliklonalne, oligoklonalne lub często monoklonalne zaburzenia limfoproliferacyjne (LPD) charakteryzujące się gorączką, uporczywym zapaleniem wątroby, hepatosplenomegalią i limfadenopatią, które wykazują różne stopnie nasilenia klinicznego w zależności od odpowiedzi immunologicznej gospodarza i miana wirusa EBV.5,6
CAEBV często towarzyszą zmiany skórne, takie jak ciężka alergia na ukąszenia komarów i choroba limfoproliferacyjna limfocytów T typu hydroa-vacciniforme (HV)., Nadwrażliwość na ukąszenia komarów (lub alergia na ukąszenia komarów, Mbh) jest unikalną skórną manifestacją zakażenia CAEBV charakteryzującą się nienormalnie intensywną reakcją miejscową w okolicy ukąszenia stawonogów związaną z objawami ogólnoustrojowymi, takimi jak gorączka, powiększenie węzłów chłonnych i zaburzenia czynności wątroby. Genom EBV występuje głównie w komórkach NK krwi obwodowej pacjentów z MBH, u których często występuje limfocytoza z komórek NK.,7-10
HV-like LPD to związana z EBV poliklonalna, oligoklonalna lub monoklonalna skórna choroba limfoproliferacyjna limfocytów T charakteryzująca się nawracającymi wykwitami pęcherzykowo-grudkowymi, głównie na twarzy i ramionach. Wykazuje szerokie spektrum agresywności klinicznej i zwykle długi przebieg kliniczny z ryzykiem rozwoju chłoniaka ogólnoustrojowego. W miarę postępu choroby u pacjentów rozwijają się ciężkie i rozległe zmiany skórne z objawami ogólnoustrojowymi, w tym gorączka, powiększenie wątroby i powiększenie węzłów chłonnych., Klasyczny HV, ciężki HV i chłoniak t-komórkowy podobny do HV stanowią continuum spektrum związanego z EBV LPD podobnego do HV.5,11-14
Ostatnio trzy wymienione powyżej Zaburzenia zostały uznane za reprezentujące spektrum limfocytów T związanych z EBV i komórek NK LPD z różnymi prezentacjami klinicznymi; jedno ogólnoustrojowe i dwa zaburzenia skórne, w tym LPD z limfocytów T podobnych do HV i MBH.14
2raporty przypadków
pacjenci opisani w dwóch poniższych przypadkach przedstawiają typowe objawy kliniczne CAEBV z MBH u dzieci. Przypadek 2 został zgłoszony wcześniej.15
2.,1
15-letni koreański chłopiec został przyjęty do szpitala z przewlekłymi okresowymi objawami dermatologicznymi i różnymi objawami ogólnoustrojowymi od piątego roku życia. Masa urodzeniowa była prawidłowa i odpowiednia dla wieku ciążowego. Podczas niedawnej wizyty na oddziale pediatrycznym wykazał odpowiedni wzrost 163,7 cm JAK na swój wiek, ale niską masę ciała 39,6 kg.
w wieku 5 lat nagle rozwinęła się gorączka, kaszel i wzdęcia brzucha. Liczba białych krwinek wynosiła 12,1 × 103/µl (limfocyty 70% , segmentowane neutrofile 21%, eozynofile 1% i monocyty 8%)., Jakościowe fluorescencyjne przeciwciała przeciwjądrowe były ujemne. Po rozpoznaniu klinicznym perforacji jelit przeszedł kolektomię subtotalną i ileostomię. Miesiąc po zabiegu, liczba limfocytów w podgrupach cytometrii przepływowej wykazywała małą liczbę limfocytów B I T, ze znacznie zwiększoną liczbą komórek NK (CD16 + CD56 + = 68%, zakres prawidłowy 5,6-31%); 1579/µl (zakres prawidłowy 100-430/µl).,
był następnie hospitalizowany pięć razy w ciągu 3 lat z powodu ostrego zapalenia gardła, infekcji górnych dróg oddechowych, zapalenia oskrzeli i zapalenia płuc oraz doświadczał nawracającej gorączki dwa lub trzy razy w miesiącu. W wieku 10 lat trafił do szpitala z powodu infekcji górnych dróg oddechowych. Splenomegalia 10,76 cm została znaleziona przypadkowo podczas badania. Od 10 roku życia intensywne reakcje skórne objawiały się w miejscach ukąszonych przez komary lub inne owady, które charakteryzowały się początkową zmianą pęcherzową, a następnie owrzodzeniem, tworzeniem skorupy i bliznami z pigmentacją (rys. 1)., Większość zmian miała
cm średnicy i często towarzyszyła im gorączka. Takie zmiany skórne występowały zazwyczaj latem oraz na kończynach górnych i dolnych. Badania laboratoryjne przeprowadzone w czasie ciężkiej alergii na ukąszenia komarów wykazały łagodne zwiększenie aktywności aminotransferazy asparaginianowej/aminotransferazy alaninowej (AspAT/alat) ze znacznym wzrostem aktywności fosfatazy alkalicznej (200 J./l) i globiny (4,5 do 4,8 g/dl).
biopsja skóry uzyskana w wyniku zmiany wskazywała na możliwość wystąpienia zespołu Sweeta. Badanie USG jamy brzusznej wykazało powiększenie śledziony., Różnice morfologiczne krwi obwodowej wykazały niskie populacje limfocytów B I T oraz limfocytozę NK . Poziom IgE w surowicy zwiększono do 20 370 J. / ml, chociaż nie stwierdzono swoistej odpowiedzi na różne bodźce alergenowe. Pomimo braku udowodnionej historii rodzinnej, jako pierwszej diagnozy różnicowej dokonano klinicznego wrażenia zespołu hiper-IgE. Przeprowadzono badania genetyczne, które obejmowały sekwencjonowanie STAT3, ale nie udało się znaleźć oczekiwanej mutacji., Biorąc pod uwagę przebieg kliniczny i limfocytozę NK, rozważano chorobę limfoproliferacyjną związaną z CAEBV lub EBV jako inne rozpoznanie różnicowe i ustalono odpowiednie testy.
testy serologiczne wykazały dodatni wynik EBV VCA-IgG, EBV-wczesnego antygenu i ujemny wynik EBV VCA IgM. Za pomocą próbki krwi pełnej, w czasie rzeczywistym ilościowe PCR dla EBV DNA wykonano w celu określenia miana wirusa we krwi(11,450 kopii / 5µl krwi pełnej). Następnie poddał się regularnej kontroli kopii genomu wirusa, która okazała się być niezmiennie wysoka, od 212.,5 kopii/µl do 1562 kopii / µl krwi pełnej. Jego problemy skórne związane z komarami lub robakami występowały sporadycznie od tego czasu, podczas gdy sporadyczne epizody choroby gorączkowej pozbawione zmian skórnych również utrzymywały się. Niespecyficzny problem skóry utrzymywał się przez 15 miesięcy. Badanie fizykalne wykazało rumieniowate do brązowawych łuszczących się plam z żółtawymi skórkami na twarzy, szyi, skórze głowy, górnej części klatki piersiowej i górnej części pleców. Był leczony miejscowo steroidami i doustnymi lekami przeciwhistaminowymi pod wrażeniem łojotokowego zapalenia skóry przez 11 miesięcy (rys. 1)., Dwa miesiące przed badaniem jego objawy pogorszyły się i odwiedził klinikę dermatologiczną. Wykonano dwie biopsje skóry twarzy i szyi oraz hybrydyzację EBV in situ. Biopsje wykazały wzrost komórek limfoplazmy w powierzchownej i głębokiej skórze właściwej z okazjonalną dystrybucją okołoodbytniczą. W większości komórek limfatycznych nie stwierdzono wyraźnej atypii. Immunohistochemia wykazała wiele komórek limfatycznych CD56+. Liczne limfocyty wykazywały pozytywną reakcję jądrową na hybrydyzację EBER in situ., Retrospektywnie, hybrydyzacja EBER in situ została zastosowana zarówno do biopsji skóry dolnej części nogi z powodu ciężkiej alergii na ukąszenia komara, jak i perforowanego jelita wyciętego 10 lat temu (rys. 2). Zidentyfikowano wiele komórek limfoidalnych z pozytywną reakcją, nie tylko w skórze, ale także w ścianie jelita i zatokach wątroby i węzła chłonnego, co potwierdziło zakażenie CAEBV alergią na ukąszenia komarów i limfocytozą NK. Pacjent był leczony zachowawczo. Dwa lata później został ponownie przeniesiony z powodu hemofagocytozy limfohistiocytozy (HLH)., Był leczony zgodnie z wytycznymi leczenia HLH-200416 i reagował przejściowo, ale później rozwinęła się perforacja jelit i zmarł na sepsę.
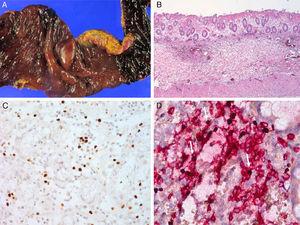
Przypadek 1. A) perforowana okrężnica w wieku 5 lat. B) wyniki mikroskopowe wykazują ostre i przewlekłe zapalenie z tkanką ziarnistą. C) hybrydyzacja EBER in situ ujawnia limfocyty EBV-dodatnie. D) limfocyty EBV-dodatnie są dodatnie dla CD3.
2.,2
10-letni koreański chłopiec trafił do oddziału dermatologii skarżąc się na intensywne reakcje skórne w miejscach ukąszeń komarów. Wykazywał liczne rozproszone, punktowane owrzodzenia na obustronnych kończynach dolnych. Oprócz wyraźnej reakcji skórnej, przez całe dzieciństwo popierał także objawy ogólnoustrojowe, w tym gorączkę po ukąszeniach owadów. Wykonano biopsję skóry i poddano miejscowemu leczeniu zmiany bez dalszej oceny ogólnoustrojowej. W wieku 16 lat pacjent przyjmował z wyczuwalną masą zlokalizowaną na lewej szyi, trwającą 2-3 tygodnie., W badaniu fizykalnym w lewej szyi znajdował się konglomerat dużych węzłów chłonnych, z których największy mierzył 7 × 5 cm. Ze względu na przebyte zmiany skórne, przeprowadzono dokładną kontrolę jego nóg, ujawniając liczne płytkie wrzody z gojącymi się bliznami. Tomografia komputerowa i pozytonowa tomografia emisyjna wykazały liczne słabo wzmacniające i o zmiennej wielkości jednorodne węzły chłonne obejmujące lewy obszar szyjki macicy i obustronne obszary pachwinowe., Ponadto występowały zmiany wieloogniskowe wykazujące zwiększone wychwyt 2-deoksy-2-fluoro-D-glukozy w skórze i podskórnej warstwie obustronnych policzków i pośladków. W badaniu hematologicznym liczba krwinek i stężenie dehydrogenazy mleczanowej mieściły się w granicach normy. Anty-VCA IgG, anty-EA i anty-EBNA IgG były dodatnie, a ANTY-VCA IgM było ujemne. Liczba kopii DNA EBV wynosiła 529,8 kopii / µl krwi pełnej.,
wykonano biopsję węzłów chłonnych, która wykazała poszerzenie parakorteksu z naciekiem heterogenicznych komórek zapalnych, w tym małych limfocytów, histiocytów i wielu eozynofilów. Naciek zapalny był przerywany przez rozproszone Duże jednojądrzaste lub wielojądrowe atypowe komórki Reed-Sternberga (RS), które miały duże eozynofilowe jądra i grubą błonę jądrową., Wykorzystując badania immunohistochemiczne, komórki podobne do RS wykazały silną błoniastą plamę dla CD30 i perinuclear barwienia dla CD15 i były dodatnie dla PAX-5 i LMP-1, ale ujemne dla CD20, CD3 i EBNA-2. Nietypowe jednojądrowe i wielojądrowe komórki RS-podobne wykazały pozytywny sygnał hybrydyzacji in situ EBER. Oprócz komórek podobnych do RS, wiele małych limfocytów rozproszonych w tle było również dodatnich dla hybrydyzacji in situ EBER. Nie stwierdzono nieprawidłowości w biopsji szpiku kostnego, z wyjątkiem kilku małych limfocytów EBV-dodatnich., Biopsja skóry z obszaru alergii na ukąszenia komarów w 2002 roku została poddana retrospektywnej ocenie, ujawniając ciężką martwicę naskórka i górnej skóry właściwej. Nie było nacieku małych limfocytów, histiocytów i wielu eozynofilów wokół naczyń krwionośnych i mieszków włosowych i światła naczyń krwionośnych były często niszczone przez czerwonych krwinek (RBC) i fibryny. Analiza immunohistochemiczna wykazała, że naciekające komórki były niejednorodne w ich rodowodzie; niektóre z nich były dodatnie dla CD3 i CD4 lub CD8 lub cytotoksycznych komórek T, podczas gdy inne były dodatnie dla komórek NK CD56., Wiele komórek EBV-dodatnich zostało udokumentowanych hybrydyzacją EBER in situ. Postawiono diagnozę przewlekłej aktywnej infekcji EBV z nadwrażliwością na ukąszenia komarów i polimorficzną limfoproliferacją symulującą chłoniaka Hodgkina. Pacjent był leczony ABVD (adriamycyna, bleomycyna, winblastyna i dakarbazyna) przez sześć cykli z całkowitą remisją. Obecnie pozostaje wolny od choroby przez 7 lat po leczeniu.,
3discussion
przebieg kliniczny pacjentów z CAEBV zależy od równowagi między czynnikami związanymi z EBV a funkcją immunologiczną gospodarza i może być tlący, postępujący lub agresywny. U niektórych pacjentów rozwija się chłoniak komórkowy EBV + t/NK / białaczka.4,17 w latach 1998-2014 w Samsung Medical Center w Korei zdiagnozowano chorobę CAEBV u 13 pacjentów w wieku 10-58 lat (mediana wieku 22 lat, dziewięciu mężczyzn i cztery Kobiety) (Tabela 1). Częstymi objawami klinicznymi były gorączka (13/13), powiększenie wątroby (9/12), powiększenie węzłów chłonnych (7/11), limfocytoza NK (3/4), MBH (4/13) i LPD podobne do HV (2/13)., U niektórych pacjentów wystąpiła perforacja jelit, pląsawica lub zawał mózgu. W medianie obserwacji trwającej 36 miesięcy, siedmiu pacjentów (54%) zmarło z powodu choroby, dwóch pacjentów (15%) miało chorobę przewlekłą, a dwóch pacjentów (17%) było wolnych od choroby. Dwóch pacjentów zostało straconych do obserwacji. Przyczyną śmierci był zespół hemofagocytarny i niewydolność narządów u czterech pacjentów, chłoniak limfatyczny T z EBV-dodatnim u jednego pacjenta oraz agresywna białaczka z komórek NK u jednego pacjenta. Limfoproliferacja linii B naśladująca chłoniaka Hodgkina, jak stwierdzono w przypadku 2, jest rzadka, ale była wcześniej zgłaszana.,18
zakażeniu CAEBV prawie zawsze towarzyszy różny stopień limfoproliferacji. Klonalność EBV i zakażonych EBV komórek T lub NK jest różna i może być poliklonalna, oligoklonalna lub monoklonalna. W miarę postępu choroby od poliklonalnej limfoproliferacji do choroby monoklonalnej, atypia histologiczna wzrasta. Ohshima i in. zaproponowano kategoryzację CAEBV na trzy grupy-polimorficzną i poliklonalną, polimorficzną i monoklonalną lub monomorficzną i monoklonalną-opartą na klonalności i zmianach histologicznych.19 w serii zgłoszone przez Ohshima i wsp.,, U 8/48 pacjentów z zakażeniem CAEBV stwierdzono poliklonalną rearanżację genu TCR, a naciekające komórki wykazywały histomorficzną histomorfologię; u 15 pacjentów stwierdzono polimorficzną morfologię i dwuklonalną lub monoklonalną rearanżację genu TCR; u 25 pacjentów wykazano monomorficzną histomorfologię i monoklonalną rearanżację genu TCR. U pacjentów z monomorficznym i monoklonalnym typem zakażenia CAEBV rokowanie było gorsze niż u pacjentów z polimorficzną chorobą poliklonalną lub polimorficzną chorobą monoklonalną. Przeżycie grup polimorficznych/poliklonalnych i polimorficznych / monoklonalnych nie różniło się znacząco., Grupy monomorficzne / monoklonalne CAEBV by Ohshima et al. może odpowiadać systemowemu LIMFOCYTOWI T LPD zgodnie z klasyfikacją WHO z 2008 roku.20
podsumowując, CAEBV jest rzadkim LPD związanym z EBV głównie z limfocytami T lub komórkami NK o szerokim spektrum prezentacji klinicznej. Rozpoznanie choroby jest ważne dla odpowiedniego postępowania z pacjentem. Analiza EBV poprzez real-time PCR próbki krwi lub EBV hybrydyzacji in situ w dotkniętej tkanki jest ważne, aby uniknąć przeoczenia tych pacjentów i powinny być włączone do głównych badań diagnostycznych dla dzieci z gorączką.,
ujawnienie etyczne
Ochrona osób i zwierząt. Autorzy oświadczają, że w tym badaniu nie przeprowadzono żadnych eksperymentów na ludziach ani zwierzętach.
poufność danych. Autorzy oświadczają, że postępowali zgodnie z protokołami swojego centrum pracy nad publikacją danych pacjenta.
prawo do Prywatności i świadomej zgody. Autorzy oświadczają, że w artykule nie pojawiają się żadne dane pacjenta.
konflikt interesów
autorzy nie deklarują żadnego konfliktu interesów.