Wat is volatiliteit?
een stof zou vluchtig zijn als zij kookt bij een lage temperatuur en van de vloeibare fase overgaat in de gasfase.
stoffen die gassen zijn bij kamertemperatuur zijn extreem vluchtig: ze hebben een hoge vluchtigheid. Ze kunnen alleen worden gezien als vloeistoffen wanneer ze worden blootgesteld aan lage temperaturen of hoge druk.
onderstaande tabel toont enkele stoffen gerangschikt in volgorde van afnemende kookpunt en toenemende vluchtigheid., In de tabel is borium de minst vluchtige stof en waterstof de meest vluchtige stof.,

Volatility and Vapor Pressure
At the molecular level, particles in liquids have a range of kinetic energies.,De meest energetische deeltjes hebben genoeg energie om uit de vloeistof te ontsnappen en de gasfase in te gaan. We zien dit als verdamping.
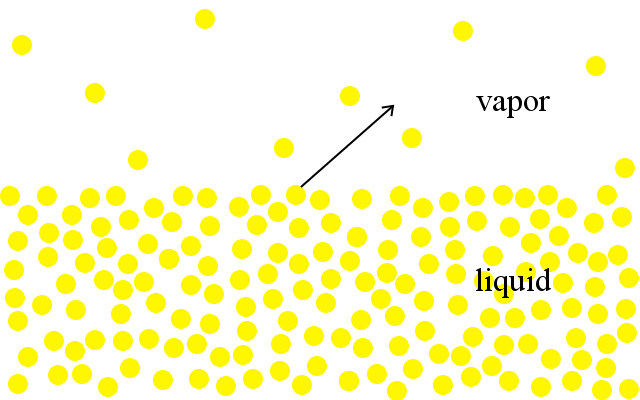
een vloeistof kookt wanneer de druk van de deeltjes die de gasfase ingaan stijgt om gelijk te zijn aan de omringende Atmosferische druk.
hoe dichter een vloeistof bij het kookpunt is, hoe hoger de dampdruk.Vloeistoffen met een laag kookpunt hebben bij een bepaalde temperatuur een hogere dampdruk dan vloeistoffen met een hoog kookpunt.daarom heeft bijvoorbeeld aceton met een kookpunt van 56 °C een hogere dampdruk dan water.,Bij kamertemperatuur zal aceton in grotere mate dan water in de dampfase terechtkomen.Dit is een kenmerk van vluchtige vloeistoffen.