Chaque année, près de 20 millions de tonnes de nitrate d’ammonium sont produites dans le monde. C’est jusqu’à présent l’engrais le plus puissant, économique et pratique sur le marché, aidant les agriculteurs à nourrir des milliards. Cependant, la récente explosion catastrophique à Beyrouth rappelle les dangers associés au stockage et au transport inappropriés de ce produit chimique commun., Comment pouvons-nous exploiter la puissance du nitrate d’ammonium tout en veillant à ce que des tragédies comme Beyrouth soient évitées à l’avenir?
La catastrophe de Beyrouth
Le 4 août 2020, une grande quantité de nitrate d’ammonium dans un hangar de stockage du port de Beyrouth a explosé, faisant plus de 300 morts et 6 000 blessés, ainsi que d’énormes dégâts matériels, laissant environ 300 000 personnes sans abri., L’explosion catastrophique de Beyrouth était l’un des rares accidents à grande échelle causés par le nitrate d’ammonium, comparable seulement aux explosions de Texas City, aux États-Unis (1947); Toulouse, France (2001); et Tianjin, Chine (2015).
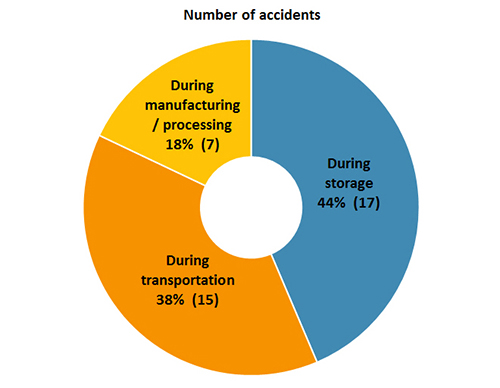
Depuis le début du 20e siècle, il y a eu près de 40 accidents majeurs, dont plus de la moitié au cours des 20 dernières années. Onze de ces accidents ont impliqué plus de 1 000 tonnes de nitrate d’ammonium ou causé plus de 30 décès (figure 1). Plus de 80% de ces accidents se sont produits pendant l’entreposage ou le transport du nitrate d’ammonium (figure 2)., L’analyse de ces accidents montre que les explosions de nitrate d’ammonium sont presque toujours précédées d’incendies ou d’autres sources d’inflammation.
Pour encore plus d’informations sur les propriétés chimiques du nitrate d’ammonium, ses dangers et les règles de sécurité téléchargez ce rapport CAS détaillé.
Le nitrate d’ammonium peut-il être apprivoisé?
Que peut-on faire pour éviter à l’avenir des tragédies comme Beyrouth? La clé pour stimuler l’innovation future dans cet espace est de comprendre la structure moléculaire et les réactions à l’origine de ces puissantes explosions., Le nitrate d’ammonium est produit par réaction de l’ammoniac avec de l’acide nitrique dans l’eau suivie d’une évaporation minutieuse de l’eau.
![]()
L’ammoniac est le plus souvent préparé à partir d’azote atmosphérique, tandis que l’acide nitrique est préparé à partir de la combustion de l’ammoniac, et donc le nitrate d’ammonium est le plus commodément fabriqué là où l’ammoniac est fabriqué. La formation de nitrate d’ammonium dégage des quantités importantes de chaleur, ainsi il est fait en solution aqueuse pour mieux dissiper cette chaleur., L’eau doit ensuite être retirée de la solution pour donner du nitrate d’ammonium solide, le plus souvent par évaporation. Bien que le nitrate d’ammonium soit stable aux températures habituelles de sa fabrication et de sa purification, des additifs sont souvent utilisés pour réduire les risques. Par exemple, des composés potassiques tels que les engrais azote-potassium et azote-phosphore-potassium ont été utilisés pour augmenter la stabilité du nitrate d’ammonium à la transition de phase et diminuer sa sensibilité à l’explosion., Des nitrates de calcium et de magnésium ont également été ajoutés au nitrate d’ammonium en petites quantités pour améliorer sa stabilité physique, mais les mélanges absorbent plus facilement l’eau de l’atmosphère. Le nitrate d’ammonium de calcium (CAN), préparé à partir de nitrate d’ammonium et de carbonate de calcium, est utilisé dans certains cas comme alternative au nitrate d’ammonium. Le sulfate d’aluminium a également été utilisé comme additif de séchage pour le nitrate d’ammonium. Bien que ces solutions de rechange aient aidé, il est important de noter que des impuretés involontaires dans le processus de fabrication peuvent réduire sa stabilité ou faciliter l’explosion.,
Nitrate d’ammonium Innovation axée sur la sécurité
Une analyse approfondie de la collection de contenu CAS révèle quelques domaines clés qui ont commencé à émerger dans le paysage de la propriété intellectuelle, soulignant les efforts visant à prévenir les explosions accidentelles ou les abus. Il s’agit notamment d’avancées concernant les mélanges, les revêtements, les formulations à libération lente, le contrôle de la taille des particules et les approches d’hygroscopicité qui minimisent le potentiel d’utilisation abusive et augmentent la stabilité pour un stockage plus sûr., Par exemple, un revêtement pour un engrais a été inventé qui empêche l’infiltration d’hydrocarbures, tels que du mazout, dans les pores de l’engrais, réduisant ainsi son efficacité en tant qu’oxydant (WO2003106377). Alternativement, des approches hygroscopiques ont également été explorées en ajoutant un ingrédient clé tel qu’un double sel d’urée qui forme un engrais stable avec du nitrate d’ammonium (US20150218058)., Ainsi, certaines alternatives ont émergé qui offrent aux utilisateurs des options sûres et rentables, mais il y a encore des compromis importants soit dans la sécurité ou la teneur en azote, donc plus d’innovation est encore nécessaire.
Recherche d’engrais azotés alternatifs
Bien que le nitrate d’ammonium soit un engrais important en raison de sa teneur élevée en azote, ses risques explosifs limitent son application et il a même été interdit dans certaines régions., Réduire la concentration de nitrate d’ammonium, trouver des composés alternatifs et développer des formes plus sûres sont des stratégies qui peuvent aider à augmenter la sécurité des engrais azotés. Le tableau 1 énumère d’autres engrais azotés qui sont apparus comme des options plus sûres qui pourraient fournir des substituts au nitrate d’ammonium. Malheureusement, l’alternative avec la teneur en azote la plus élevée est l’ammoniac anhydre, qui est un gaz toxique à température ambiante., D’autres solutions de remplacement à haute teneur en azote, telles que les solutions d’hydroxyde d’ammonium et l’urée, sont attrayantes en raison de leur faible coût et de leur efficacité; cependant, elles sont volatiles. Des formulations à libération lente d’urée, ainsi que des lignines et des hydrogels modifiés, ont été développées pour surmonter ce défi.
Tableau 1., List of alternative nitrogenous fertilizers
|
Fertilizer |
Comment |
|
|---|---|---|
|
Anhydrous ammonia |
Pressurized gas, Risk Management Plan (RMP)-regulated substance with a threshold of 10,000 lbs, regulated as Dangerous Goods for transportation.,div id= »8648a5f2f4″> Sodium nitrate |
Stable |
|
Calcium cyanamide |
Contains calcium |
|
|
Calcium nitrate |
Contains calcium |
Handling ammonium nitrate safely
Previous disasters have heightened public awareness of the explosive nature of ammonium nitrate, and the consequences of its unsafe storage and use., En réponse, de nombreux règlements, règles et directives concernant le nitrate d’ammonium, en particulier en ce qui concerne son stockage et sa manipulation, ont vu le jour dans différents domaines pour améliorer la sécurité. Les principaux règlements américains pour le nitrate d’ammonium sont » OSHA 29 CFR 1910.109 (i) – Stockage du nitrate d’ammonium”, et le Mémorandum de « Guidance on the Ammonium Nitrate Storage Requirements in 29 CFR 1910.109(i)” publié en 2014 après le Adair Grain Inc., Explosion de la société DBA West Fertilizer en 2013., Il convient cependant de noter que l’application diligente des règles et règlements de sécurité est la clé pour éviter de futurs accidents tels que la catastrophe de Beyrouth., peut être résumé comme suit
(Figure 3):
- Ventilation: capable d’une ventilation adéquate en cas d’incendie
- Isolation de la combustion: des matériaux non combustibles et résistants à l’AN sont nécessaires
- Contrôle de la température: les températures de stockage doivent être inférieures à 130℉
- Volume: les limites de stockage doivent stockage à partir d’autres produits
Malgré les problèmes de sécurité, le nitrate d’ammonium reste un engrais important dans le monde entier car il est efficace, bon marché et facile à fabriquer. Cependant, comme cela a été souligné une fois de plus par l’incident de Beyrouth, la vulnérabilité du nitrate d’ammonium aux incendies et aux explosions en raison de mauvaises pratiques de stockage ou de la contamination présente des risques importants., Des réglementations incohérentes et un manque de sensibilisation durable sur la façon de manipuler et de stocker en toute sécurité le nitrate d’ammonium dans la chaîne d’approvisionnement mondiale sont des défis clés qui doivent être surmontés par l’éducation et le plaidoyer pour éviter une nouvelle tragédie mondiale.
Découvrez comment les scientifiques rendent le nitrate d’ammonium plus sûr dans notre plus récent livre blanc Leçons apprises du nitrate d’ammonium.