Introduction
Le carcinome kystique adénoïde (ACC) est une tumeur rare se produisant principalement dans les glandes salivaires (glandes parotides, glandes sous-maxillaires, glandes sublinguales et glandes salivaires mineures).1,2 ACC rarement peut également apparaître dans d’autres sites du corps,y compris les glandes lacrymales,3 système respiratoire supérieur,4-5 sein, 6 prostate7 et les organes reproducteurs bas féminins.8 L’ACC primaire dans le foie est extrêmement rare avec un seul cas ayant été rapporté dans la littérature.,9 Nous présentons ici un cas inhabituel d’ACC dans le foie sans tumeur trouvée dans d’autres organes, à l’exception de l’atteinte du diaphragme et de l’épiploon adjacents. Nous favorisons qu’il s’agisse d’un carcinome kystique adénoïde primaire dans le foie. Nous avons effectué des analyses histopathologiques et immunohistochimiques et fourni des informations sur le traitement et le suivi.
Rapport de cas
Il s’agit d’un homme de 44 ans présentant une distension abdominale supérieure pendant trois mois et des douleurs abdominales supérieures pendant une semaine. L’examen physique a révélé que le foie s’étendait jusqu’à 10 cm au-delà du contour des côtes. Aucune sensibilité hépatique n’était présente., L’examen physique n’a révélé aucun ictère ou angiome d’araignée (naevus d’araignée). Il n’y avait pas d’œdème dans son corps. Les ganglions lymphatiques superficiels n’étaient pas palpables. L’échographie a montré un foie anormal avec une masse dans le lobe gauche avec un signal d’écho mixte et aucune augmentation du flux sanguin (Figure 1A). Un examen tomographique informatisé ultérieur (Figure 1B) a révélé une masse de 21,0 x 16,0 cm avec une bordure irrégulière dans le lobe gauche du foie. Sa numération globulaire complète, sa bilirubine totale et ses taux de protéines se situaient tous dans les limites normales., Les enzymes hépatiques alanine transaminase (ALT) et aspartate aminotransférase (ASAT) se situaient dans les plages normales, mais la gamma-glutamyl transférase (GGT) était élevée (155 U/L, plage normale 7-50 U/L). Son test HBsAg était négatif. Les taux sériques d’AFP et de CEA se situaient dans les limites normales. CA19, 9 a été élevé à 108,6 U/mL (normale 0-30 U/mL).
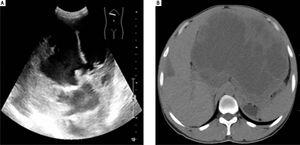
L’échographie (A) a révélé une masse d’écho mixte dans le lobe gauche du foie et la tumeur était trop grande pour être mesurée par cette méthode., L’examen tomographique informatisé (B) a révélé une masse importante d’environ 21,0 cm x 16,0 cm avec une densité mixte et une bordure irrégulière dans le lobe hépatique gauche.
La préopératoire diagnostic clinique était un cancer primaire du foie et une intervention chirurgicale est prévue. Au cours de l’opération, une énorme tumeur du foie a été trouvée dans le lobe hépatique gauche avec invasion dans la capsule hépatique et adhérant au diaphragme. Le lobe gauche du foie avec la capsule et le diaphragme adjacents a été réséqué., Une partie de l’épiploon a également été réséquée.
Le tissu hépatique réséqué mesurait 24,0 x 20,0 x 12,0 cm et le sectionnement a révélé une masse de 22,0 x 18,0 x 11,0 cm. La masse avait une surface de coupe solide et kystique avec une bordure floue. Au microscope, la tumeur a montré un modèle de croissance principalement cribriforme (surface de 90%) avec une composante mineure de modèle de croissance tubulaire et solide (Figure 2). Les pseudocystes / pseudoglands dans les zones cribriformes ont été remplis de matériau membranaire de base lâche myxoïde à éosinophile dense (Figure 2B et Figure 2C)., Il y avait parfois de véritables petites structures glandulaires dans les zones cribriformes (figure 2C). Une composante mineure de la croissance solide (Figure 2D) et des structures tubulaires (Figure 2E) était présente. Le stroma a montré une hyalinisation abondante qui a étranglé les cellules tumorales en trabécules anastomosées (Figure 2F). Les cellules tumorales avaient des noyaux hyperchromatiques ovales à angulés avec peu de cytoplasme et une bordure cellulaire indistincte. Il y avait un pléomorphisme nucléaire léger (figure 2). Le nombre de mitoses était de 1/10 champs de puissance élevée et il n’y avait pas de mitose atypique. Une nécrose focale des cellules tumorales était présente (5%)., Immunohistochimiquement, les cellules luminales et abluminales ont montré une positivité diffuse pour CK7 et CK19, et leur intensité de coloration était plus forte dans les cellules luminales que dans les cellules abluminales (Figure 3A). La cytokératine CK8 / 18 était diffuse positive dans les cellules luminales, mais seulement focale faiblement positive dans les cellules abluminales. La coloration P63 a marqué les cellules abluminales mais pas les cellules luminales (Figure 3B) alors que CD117 a montré un motif de marquage opposé (Figure 3C). La prolifération du Ki-67 était d’environ 10 à 15% (figure 3F).,
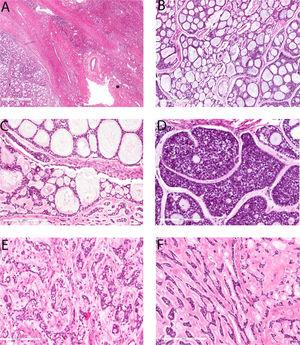
Figure 2. Caractéristiques microscopiques du carcinome kystique adénoïde hépatique primaire. Il y a une capsule épaisse entre la tumeur (inférieure gauche) et le tissu hépatique adjacent (supérieur droit, A, 20x). Le modèle de croissance prédominant de cette tumeur est cribriforme (B, 100x). Les espaces kystiques dans la zone cribriforme sont principalement des pseudocystes remplis de matériau myxoïde lâche (B, 100x) et de matériau membranaire à base éosinophile (C, 200x), mais il y a parfois de vraies petites glandes (C, 200x)., Cette tumeur ne contient que la croissance solide focale (D, 200x) et les structures tubulaires (E, 200x). Il y a une hyalinisation abondante dans le stroma dans certaines zones qui ont comprimé les cellules tumorales en brins d’anastomose (F, 200x).
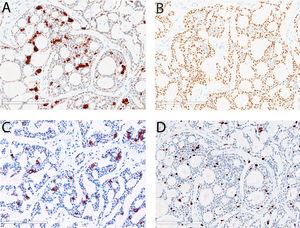
Résultats de coloration immunohistochimique du carcinome kystique adénoïde hépatique primaire., La cytokératine 7 est diffuse positive dans les cellules tumorales et présente une coloration plus forte dans les cellules luminales que les cellules abluminales (A, 200x). La coloration P63 marque les cellules abluminales mais pas les cellules luminales (B, 200x). La coloration CD117 marque les cellules luminales mais pas les cellules abluminales (C, 200x). L’indice de prolifération Ki-67 dans cette tumeur est d’environ 10-15% (D, 200x).
Selon les critères diagnostiques les plus récents de l’Organisation mondiale de la Santé (OMS), les principaux critères histologiques diagnostiques pour l’ACC comprennent la population de cellules biphasiques (cellules luminales et abluminales) et des modèles de croissance variables, y compris les tubules, l’architecture solide et cribriforme.10 La tumeur dans notre cas a démontré une population de cellules biphasiques avec une croissance principalement cribriforme avec des structures solides et tubulaires focales. Par conséquent, cette tumeur remplit les critères histologiques pour ACC.,10 Le diagnostic histologique a été confirmé par des taches immuno-histochimiques qui ont marqué deux populations cellulaires distinctes (cellules luminales CK8 / 18 diffuses+, p63-, CD117+; cellules abluminales CK8 / 18 focales +, p63 +, CD117-).
Cette tumeur a également envahi la capsule hépatique et impliqué le diaphragme adjacent. L’épiploon contenait également plusieurs nodules tumoraux allant de 1,2 à 5,4 cm. La tumeur du diaphragme et de l’épiploon présentait des caractéristiques histologiques similaires à celles du foie.,
Après le diagnostic de carcinome kystique adénoïde, le patient a subi une TEP-TDM du corps entier qui n’a révélé aucune tumeur dans d’autres sites du corps, y compris les glandes salivaires, les autres sites de la tête et du cou, les poumons et la prostate, etc. Sur la base de ces résultats, sa tumeur du foie était plus compatible avec un carcinome kystique adénoïde hépatique primaire.
Après la chirurgie, le patient a refusé de recevoir une chimiothérapie et une radiothérapie en raison de problèmes financiers., Sur son lobe de suivi à 26 mois après la chirurgie, l’imagerie par résonance magnétique a montré une récidive tumorale dans le lobe droit de son foie, du diaphragme, de l’épiploon et du rétropéritoine. Il n’y a pas eu de maladie dans d’autres sites du corps lors des études d’imagerie. Le patient est décédé de maladie à 33 mois après la chirurgie.
Discussion
Dans ce rapport, nous avons présenté un cas unique d’ACC dans le foie. La tumeur a envahi la capsule hépatique et a également impliqué le diaphragme et l’épiploon adjacents., Ce patient n’avait pas de tumeur dans d’autres sites, y compris la région de la tête et du cou, les voies respiratoires supérieures et les voies génitales au moment de la présentation initiale et du suivi à 26 mois de l’étude d’imagerie. Cette tumeur a démontré des caractéristiques morphologiques typiques et un profil immunohistochimique de l’ACC, selon les critères de l’OMS.10 Ce cas a été examiné lors de la conférence de consensus ministérielle et a également été vu par deux pathologistes en consultation dans deux autres hôpitaux extérieurs.,
Le carcinome kystique adénoïde est une tumeur relativement rare, le plus souvent dans les glandes salivaires, mais il peut également se produire dans d’autres sites du corps, y compris les voies aérorespiratoires supérieures, le sein et les voies génitales, etc. Il est très rare comme une tumeur pri mary dans d’autres sites. Dans le foie, un seul carcinome kystique adénoïde primaire a été rapporté dans la littérature anglaise.9 La patiente dans cette étude9 était une femme de 21 ans qui présentait une masse de 30 cm pendant sa grossesse. La tumeur occupait presque tout le foie. Dans notre cas, la tumeur avait une taille de 21 cm., Dans le foie, la tumeur peut atteindre une grande taille probablement en raison de l’emplacement intra-abdominal qui peut donner à la tumeur plus d’espace pour se développer avant que les symptômes ne deviennent évidents.
Nous privilégions notre cas est un ACC primaire du foie. Notre cas est le deuxième cas d’ACC primaire dans la littérature. Nous privilégions un ACC primaire du foie basé sur les faits suivants. Premièrement, cette tumeur a formé une seule masse dans le foie au moment de la chirurgie initiale et il n’y avait aucune preuve de tumeur dans aucun autre organe, y compris les poumons et les glandes salivaires à ce moment-là. Les métastases forment généralement de multiples nodules dans le foie., Deuxièmement, lors de son suivi à 26 mois (avec étude d’imagerie), il n’y avait toujours pas de tumeur dans un autre organe sauf récidive dans le foie, le diaphragme, l’épiploon et le rétropéritoine. Troisièmement, d’autres types de tumeurs de type glande salivaire ont été signalés comme des tumeurs primaires dans le foie et le système biliaire, y compris le carcinome mucoépidermoïde, le carcinome myoépithélial et le carcinome épithélial-myoépithélial.11-17 Carcinome mucoépidermoïde primaire a également été rapporté dans le pancréas et le côlon ascendant.,18,19 Il y a deux explications possibles pour l’histogenèse des tumeurs primaires de type glande salivaire dans le foie, le tractus pancréatobiliaire et le tractus intestinal:
- •
Les cellules souches / réserves se transdifférencient en tumeurs salivaires de type glnd au cours de la transformation maligne (plus probable).19
- •
Ces tumeurs peuvent provenir du tissu des glandes salivaires ectopiques.
L’hétérotopie / choristome des glandes salivaires est généralement observée dans la région de la tête et du cou, mais elle peut être observée dans le tractus gastro-intestinal, y compris l’œsophage, l’intestin grêle, le côlon et le rectum.,20-23 Jusqu’à présent, aucune hétérotopie/choristome des glandes salivaires n’a été signalé dans le foie et le système biliaire, mais cette possibilité ne peut être entièrement exclue.
Le diagnostic différentiel majeur pour notre cas est un carcinome kystique adénoïde métastatique provenant d’un autre site. Parmi les carcinomes kystiques adénoïdes dans la région de la tête et du cou, un pourcentage important d’entre eux (20 à 50%) développera des métastases à distance au moment de la présentation ou au cours de l’évolution ultérieure de la maladie.,24-27 Le poumon est le site le plus commun de métastase suivi de l’os tandis que le cerveau et le foie sont des sites beaucoup moins communs pour les métastases.Le foie 24-30 est rarement le seul site de métastase.24-30 Métastases hépatiques peuvent être le premier signe de présentation.15-16 Outre le carcinome kystique adénoïde des glandes salivaires,le carcinome kystique adénoïde provenant d’autres sites tels que la vulve31,la trachée32, la glande lacrymale33 a également été rapporté pour métastaser au foie. Notre patient n’avait pas de tumeur dans d’autres sites lors des études d’imagerie au moment du traitement et du suivi (26 mois après la chirurgie)., Ces résultats favorisent le diagnostic d’un ACC hépatique primaire comme discuté ci-dessus.
Le carcinome kystique adénoïde est une tumeur à croissance lente, mais il montre une maladie implacable et progressive avec un taux de survie à 10 ans inférieur à 50%.27 la Chirurgie est le traitement principal. La radiothérapie postopératoire est recommandée si la marge chirurgicale positive. En raison d’une mauvaise réponse, la chimiothérapie n’était généralement pas recommandée comme option thérapeutique.27 Le stade tumoral et le grade histologique sont les deux facteurs pronostiques les plus importants du carcinome kystique adénoïde dans la région de la tête et du cou.,26,27,34 Un modèle de croissance solide était associé à un pronostic plus mauvais.26,27,34 Notre cas a montré une croissance solide très focale (
En résumé, nous avons présenté un cas unique d’ACC chez un patient mâle de 44 ans dans son foie et nous privilégions qu’il s’agisse d’un ACC hépatique primaire. Le carcinome a démontré un profil morphologique et immunohistochimique typique du carcinome kystique adénoïde.
Abréviations
- •
ACC: carcinome kystique adénoïde.
- •
ALT: alanine transaminase.
- •
ASAT: aspartate aminotransférase.
- •
GGT: gamma-glutamyl-transférase.,
Conflit d’Intérêts
Les auteurs déclare qu’il n’y a pas de conflit d’intérêt concernant la publication de cet article.
Financement
Ce travail a été soutenu par la Fondation Nationale des Sciences Naturelles de Chine (No 81370661) et la Fondation des Sciences Naturelles de la Province chinoise du Henan (No 102300410038).