L’aura visuelle représente un type de déficit neurologique familier à tout praticien de soins oculaires. Bien que précédant classiquement la migraine ou la crise, une aura, simplement définie, est un symptôme, pas une condition médicale en soi. De même, des termes tels que scotomes visuels, amaurosis fugax ou obscurcissements visuels transitoires représentent également une perturbation de la vision; cependant, ils ne précèdent pas classiquement les céphalées migraineuses ou les crises corticales et sont associés à d’autres types de pathologie., Néanmoins, chaque terme, lorsqu’il est utilisé dans les bonnes circonstances, peut définir remarquablement similaire déficits visuels dans un ou deux yeux.
Une liste importante de différences doit être considérée lorsqu’un patient décrit de tels troubles visuels, certains associés à une morbidité importante. Pour cette raison, la plainte d’aura visuelle ou de scotome nécessite une évaluation complète et ne doit pas simplement être supposée migraineuse (un diagnostic d’exclusion)., Une compréhension des différents types d’aura et de scotomes et de leur présence permet aux praticiens des soins oculaires de différencier les causes et d’ordonner des tests appropriés pour des pathologies potentiellement très différentes.

Présentation et pathogenèse
Les auras visuelles ou les scotomes ne sont pas flous., Une aura visuelle est une perturbation perceptuelle visuelle transitoire ou de longue date, accompagnée d’une migraine ou d’une crise, pouvant provenir de la rétine ou du cortex occipital. Les changements visuels décrits par les patients sont souvent appelés flou, un mot abusé par les patients aussi fréquemment que le mot « étourdi. »Le flou a des significations connotatives différentes pour les patients. L’Aura peut être définie positive (voir quelque chose qui n’est pas là) ou négative (ne pas voir quelque chose qui est là). De plus, une image réelle peut être falsifiée (apparaît plus grande, persévère,etc.). Les auras visuelles peuvent être transitoires (e.,g., quelques secondes) ou de longue date (peut-être pendant des mois) et, surtout, ils peuvent être accompagnés de maux de tête ou d’autres types d’aura tels que vertiges, engourdissements, picotements ou aphasie.
La définition du scotome visuel est similaire à celle de l’aura visuelle. Les différentiels pour le scotome incluent également la migraine et les convulsions, mais le terme est plus approprié lié à l’ischémie, aux dégénérescences et inflammations rétiniennes, aux syndromes paranéoplasiques et à d’autres troubles neurologiques., Pour les scotomes visuels, la pathogenèse primaire peut se produire au niveau des récepteurs, de l’arbre artériel rétinien, des artères ciliaires postérieures courtes, de l’artère ophtalmique, du nerf optique, de l’artère carotide, de l’artère vertébrobasilaire ou de l’hémisphère cérébral.
Les types migraineux d’AURA n’impliquent en fait aucune pathologie tissulaire détectable ainsi que peu ou pas d’attente de déficit permanent; cependant, la migraine avec AURA a démontré un risque accru d’accident vasculaire cérébral.1 Les causes ischémiques, à condition que le seuil ischémique ne soit pas significativement dépassé, bénéficient d’une récupération totale., D’autres causes de scotome visuel peuvent être auto-limitées ou nécessiter une intervention importante pour prévenir une morbidité ou une mortalité supplémentaires.
Causes rétiniennes
L’aura qui provient de la rétine se présentera uniquement sous la forme d’un scotome non formé ou d’un défaut visuel positif ou négatif. Au niveau rétinien, les images formées ne sont pas possibles.2 Bien que techniquement l’aura puisse inclure une macropsie ou une micropsie, au niveau de la rétine, cela se produirait avec des changements spécifiques et généralement démontrables tels qu’un œdème maculaire ou une maculopathie à la cellophane, et ce ne serait pas de nature transitoire.,3 Les causes transitoires de micropsie ou de macropsie se produisent autrement corticalement.
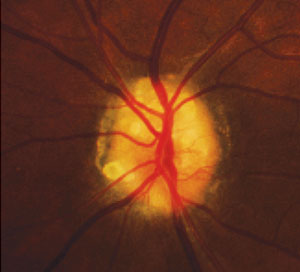
Nerf optique drusen visible à la surface du nerf chez une femme de 32 ans. Photo: Denise Goodwin, OD.
Aura au niveau de la rétine est susceptible d’être unilatérale dans la présentation, mais cela peut être difficile à élucider à partir de l’histoire du patient. L’unilatéralité est pratiquement essentielle pour attribuer l’aura à la rétine. En moyenne, l’aura rétinienne dure jusqu’à une heure et est le plus souvent embolique et rarement migraineuse.,
Une aura visuelle négative considérée comme secondaire à l’embolisation est communément appelée amaurosis fugax. Le groupe d’étude Amaurosis Fugax a défini cinq classes distinctes de cécité monoculaire transitoire en fonction de leur cause supposée: embolique, hémodynamique, oculaire, neurologique et idiopathique.4 L’absence de vision peut ou non progresser dans le champ visuel. La migraine rétinienne peut entraîner le même type de déficit visuel (aura négative); cependant, un scotome positif ou une cécité est également possible., Notez que les migraines rétiniennes sont souvent, mais pas toujours, associées à des maux de tête du même côté que le déficit visuel en une heure. Les événements emboliques peuvent également être associés ou non à des maux de tête.
Les événements ischémiques rétiniens sont plus probables chez les personnes âgées ayant des antécédents de maladie cardiovasculaire/hypertension.5 Dans une certaine mesure, les coagulopathies ou les syndromes d’hyperviscosité peuvent également être complices et nécessiter un examen si une source d’emboles n’est pas identifiée.6 Les patients plus jeunes sans antécédents de maladie cardiovasculaire sont plus susceptibles de souffrir de migraine., Étant donné que la perte de vision transitoire monoculaire localisée à la rétine (appelée amaurosis fugax) peut avoir de nombreuses causes, un historique de cas méticuleux est important. Il est essentiel que les patients et leur interniste soient conseillés par le fournisseur de soins oculaires concernant les tests appropriés pour aider au diagnostic d’un différentiel potentiel important. Encore une fois, notez que la migraine est un diagnostic d’exclusion.
Des scotomes non migraineux associés à la rétine peuvent également survenir au niveau des photorécepteurs / EPR. La rétine dans un état de repos est dépolarisée. L’état de dépolarisation nécessite de l’énergie., La maladie de l’EPR en particulier peut interférer avec la production d’énergie, ce qui peut entraîner des zones localisées d’hyperpolarisation constante des bâtonnets et des cônes affectés. En conséquence, un scotome scintillant ou pétillant constant peut se produire et peut durer des mois ou des années.7 Scotomes mousseux continus positifs ont été rapportés avec des conditions telles que la rétinopathie associée au cancer, la rétinite pigmentaire ou d’autres dégénérescences/inflammations rétiniennes telles que le syndrome du point blanc évanescent multiple ou l’élargissement de l’angle mort idiopathique.,8-10
Souvent, les troubles rétiniens se révèlent ophtalmoscopiquement; cependant, un dysfonctionnement définitif au niveau de l’EPR / des photorécepteurs peut nécessiter un test ERG multifocal car l’apparence du fond d’œil ainsi que l’angiographie à la fluorescéine peuvent être normaux. La rétinopathie associée au cancer (CAR) peut entraîner la perception de nuages tourbillonnants de fumée et de faibles éclairs de lumière occasionnels.11 Sur le plan ophtalmologique, l’apparition précoce du fond d’œil est normale, mais le test ERG peut révéler un dysfonctionnement important des bâtonnets et des cônes.,
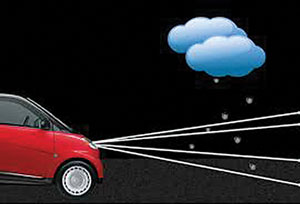
La CAR est un syndrome paranéoplasique dans lequel les auto-anticorps sont dirigés vers le néoplasme mais attaquent également des sites spécifiques de la rétine, entraînant éventuellement une atténuation de l’artériole, des marbrures de l’EPR et une pâleur discale. Il est le plus souvent associé au carcinome pulmonaire à petites cellules, mais a été décrit avec d’autres tumeurs malignes telles que les cancers du sein, gynécologiques et de la prostate., La tomodensitométrie de la poitrine ou du corps entier peut être suggérée chez des patients autrement en bonne santé pour révéler la formation de tumeurs.
Les patients présentant de tels troubles affectant la fonction du cône ont tendance à voir pire en pleine lumière (héméralopie), ce qui est souvent cliniquement contre-intuitif. Les plaintes des patients d’éblouissement et de photophobie (acquise) sont courantes avec la maladie du cône. La maladie des tiges, cependant, est associée à des difficultés de vision nocturne (nyctalopie). Les patients se plaignant de difficultés de vision diurne et nocturne nécessitent un test ERG multifocal, qui peut révéler un dysfonctionnement même en l’absence d’aura visuelle., Les photopsies sont simplement liées à l’interaction vitréorétinienne.
Maladie du nerf optique
Au niveau du nerf optique, une perte de vision non migraineuse peut survenir avec des troubles associés à une artère rétinienne centrale ou à une artère postérieure courte. En outre, le drusen du nerf optique ou l’œdème papillaire peuvent également être associés à l’aura.
En règle générale, la maladie du nerf optique produit des scotomes non formés qui sont négatifs et rarement positifs.,2 La maladie embolique bloquant l’artère rétinienne centrale ou immédiatement à la bifurcation produit un scotome négatif qui est diffus ou altitudinal, respectivement. Le déficit peut se produire pendant quelques secondes ou jusqu’à 20 à 30 minutes. Rarement, l’aura est positive et peu susceptible de marcher. Bien que tentant de classer les attaques d’amaurosis fugax comme emboliques, les fournisseurs de soins oculaires doivent toujours garder à l’esprit l’artérite, où la pathogenèse peut impliquer l’artère ophtalmique ou l’une de ses branches.,
Les études cardiaques, carotides et autres doivent être accompagnées d’un taux de sed et d’une protéine C-réactive, en particulier chez les patients de plus de 50 ans12.L’intention est d’exclure l’artérite et le potentiel de neuropathie optique ischémique artéritique. La maladie ciliaire postérieure courte est typiquement inflammatoire parce que ces vaisseaux ne sont pas anatomiquement sensibles à la maladie embolique.13 La maladie non artéritique entraînant une neuropathie optique ischémique antérieure est considérée comme secondaire à une maladie artériolarsclérotique ou même éventuellement à une dysrégulation vasculaire; cependant, la physiopathologie exacte est inconnue.,14,15
Les patients fortement suspectés d’artérite temporale doivent immédiatement être placés sous 60 mg à 80 mg de prednisone par voie orale et envoyés à un laboratoire pour des tests de taux de sed et de protéine C réactive. Les tests de laboratoire ne seront pas affectés pendant plusieurs jours après le début du traitement par la prednisone et ne révéleront pas de taux de sed faux négatif ou de protéine C réactive.16 Le traitement par la prednisone est fourni dans le but de prévenir la neuropathie optique ischémique artéritique et la cécité immédiate, qui est une conséquence réelle de l’artérite et peut survenir à tout moment., L’artérite est l’une des causes les plus fréquentes de perte de vision évitable si elle est détectée et doit toujours être suspectée chez les patients présentant une perte de vision transitoire centrale, altitudinale ou les deux.
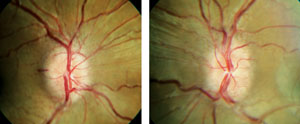
Note bilatérales, symétriques l’apparition d’un œdème papillaire. Photo: Denise Goodwin, OD.
La congestion de la tête du nerf optique peut également entraîner une atténuation transitoire de la vision, en particulier avec des changements posturaux., Les drusen du nerf optique sont des lésions occupant de l’espace qui entraîneraient un certain degré de congestion discale pouvant produire des défauts de champ persistants définis, des scotomes négatifs ou les deux qui peuvent varier considérablement (10 à 15 secondes jusqu’à quelques heures) et sont souvent précipités avec des changements posturaux.17
Les drusen Disc sont souvent diagnostiqués à tort comme un œdème papillaire parce que leur évaluation à la présidence ressemble souvent à un œdème papillaire. Les indices de diagnostic de disc drusen comprennent la présence d’une pulsation veineuse spontanée, une ramification anormale des artériels (trifurcations), ainsi que des changements pigmentaires péripapillaires., Des hémorragies peuvent être présentes et sont plus profondes et concentriques. L’autofluorescence du disque drusen peut être démontrée avec la photographie à filtre bleu. Les drusen enterrés sont mieux visualisés avec des ultrasons pour révéler les corps hyalins dans la tête nerveuse; la tomodensitométrie sans contraste est également utile, tout comme l’OCT, pour différencier le drusen du disque optique du papilledema.18
Bien que possédant une pathogenèse entièrement différente, le papilledema peut également entraîner des scotomes visuels négatifs (secondes à heures) qui peuvent également se produire avec des changements posturaux dans un ou les deux yeux, semblables à disc drusen.,19
Les patients présentant un véritable œdème papillaire présenteront classiquement des disques optiques bilatéraux gonflés ou élevés avec des marges discales indistinctes, bien qu’un œdème papillaire unilatéral avec des pressions d’ouverture allant jusqu’à 350 mm ait été enregistré, ce qui confond le diagnostic.20 Les patients atteints d’œdème papillaire peuvent être entièrement asymptomatiques, tout comme les patients atteints de disc drusen, ne révélant aucun changement visuel ou significatif du champ. Les patients atteints de papilledema et de disc drusen peuvent avoir une hypertrophie de l’angle mort dans les deux yeux, ce n’est donc pas une caractéristique différenciante.,21,22 Typiquement, les patients avec l’oedème papillaire ne démontreront aucune pulsation veineuse spontanée en raison de la pression céphalo-rachidienne accrue (typiquement > 250mm H2O). Lorsqu’ils sont interrogés, les patients peuvent être enclins à décrire des antécédents récents de maux de tête, en particulier au réveil.23 Les hémorragies, si elles sont présentes, ont tendance à être superficielles dans la couche de fibres nerveuses et les veinules peuvent révéler une congestion passive.
Le papilloedème est considéré comme l’une des véritables urgences oculaires et les patients doivent être transportés directement à l’hôpital en cas de suspicion., D’autres pathologies compartimentales ou « hydrauliques” entraînant une compression au sommet de l’orbite peuvent également entraîner des obscurcissements visuels posturaux; par conséquent, la maladie orbitale doit également être gardée à l’esprit.24
Dysfonctionnement vertébrobasilaire
L’ischémie transitoire affectant la circulation vertébrobasilaire a tendance à produire des scotomes bilatéraux négatifs, mais parfois un patient peut présenter un scotome positif. Le phénomène visuel positif est souvent décrit comme « la neige qui tombe à travers le faisceau d’un phare., »Comme d’autres crises ischémiques transitoires, le phénomène visuel peut durer plusieurs minutes ou plus et peut être associé à d’autres signes vertébrobasilaires tels qu’une conscience réduite, une diplopie, des acouphènes, des vertiges ou une dysarthrie.7
Bien que les épisodes migraineux puissent être associés aux mêmes déficits, comme la plupart des syndromes migraineux, les maux de tête suivront en moins de 60 minutes et tout déficit se résoudra entièrement en 60 minutes. Le déficit visuel est encore probablement un type de scotome scintillant ou fortifiant, même s’il est migraineux., En raison de la similitude des symptômes et du potentiel de récupération avec l’un ou l’autre mécanisme, une évaluation neurologique et cardiovasculaire est justifiée lors de l’apparition initiale.
Atteinte de l’hémisphère cérébral
Le plus souvent, l’aura visuelle qui se produit à la suite d’une maladie cérébrale est embolique, migraineuse ou liée à une crise. Aura corticale sera bilatérale et peut durer de quelques secondes à une heure. Selon l’emplacement (pariétal, temporal ou occipital), l’aura occupera cette partie du champ visuel proportionnelle au lobe affecté.,
Encore une fois, les événements ischémiques sont susceptibles de produire un scotome ou une aura négative et non mars. L’aura migraineuse est plus susceptible d’être positive (souvent décrite comme scintillante) et, en règle générale, marchera. Cette aura visuelle peut ou non être accompagnée de maux de tête. Dans le cas de l’ischémie, les maux de tête surviennent généralement lors de l’apparition de l’aura et le déficit visuel est généralement négatif. Avec la migraine, l’aura est accompagnée ou suivie dans les 60 minutes par des maux de tête.24 Si les zones d’association visuelle (c.-à-d.,, centres de vision supérieure) sont affectés, les phénomènes potentiels qui peuvent se produire comprennent la pallinopsie, la macropsie, la micropsie et les hallucinations visuelles formées. Les crises affectant l’occipital ou parfois le lobe temporal peuvent également provoquer des hallucinations visuelles non formées (cercles colorés), mais peuvent également entraîner des hallucinations visuelles formées.7 L’activité convulsive est susceptible d’être associée à d’autres phénomènes convulsifs, tels qu’une déviation oculaire ou un clignotement rapide.
Outre les maux de tête, d’autres déficits neurologiques peuvent accompagner l’aura visuelle., Avec la migraine, les vagues de dépression qui s’étendent hors du cortex visuel se produiront généralement en amont, affectant la sensation ou la force motrice. Chaque nouveau déficit peut durer jusqu’à 60 minutes. Par conséquent, l’aura visuelle initiale peut être suivie d’une atteinte pariétale (engourdissement et picotements) puis d’une atteinte frontale (faiblesse motrice). Ce processus devrait prendre jusqu’à 180 minutes (3×60). Comme c’est typique avec la migraine, les déficits devraient marcher et les maux de tête peuvent survenir à tout moment dans les 60 minutes après le début de la première aura., Classiquement, les événements ischémiques n’entraînent aucune marche et le mal de tête est le plus susceptible de survenir au début de la perte de vision. Une exception à l’aura visuelle conventionnelle est la complication de la migraine » aura persistante sans infarctus. »Dans ce cas, l’aura visuelle persistante-généralement bilatérale-restera pendant au moins une semaine et peut-être des mois ou des années sans preuve de lésion ischémique.25 La confirmation est déterminée avec des études d’imagerie, qui restent négatives.
le Dr, Banyas pratique dans un cadre d’optométrie d’entreprise et fournit des soins oculaires à plus de 15 établissements de soins infirmiers dans la grande région de Pittsburgh.
1. deFalco FA. Migraine avec aura: Quels patients sont les plus à risque d’AVC? Neurol Sci. 2015 Mai: 36 Suppl 1: 57-60.
2. Ettinger AB, Veisbrot DM, eds. Diagnostic Différentiel Neurologique: Une approche basée sur les cas. Cambridge, new york: Cambridge University Press, 2014.
3. Wiecek E, Lashkari K, Dakin S, Bex P. Roman évaluation quantitative de metamorphopsia dans la maculopathie. Investir Ophthalmol Vis Sci. 2015 Jan:56 (1): 444-504.
4. L’Amaurose Fugace Groupe D’Étude., La gestion actuelle de amaurose fugace. Coup. 1990 Fév; 21 (2): 210-8.
5. Callizo J, Feltgen N, Pantenburg S, et coll. Facteurs de risque cardiovasculaire dans l’occlusion de l’artère rétinienne centrale: résultats d’un examen médical prospectif et standardisé. Ophthalmol. Le 9 juillet .
6. Schockman S, Glueck CJ, Hutchins RK, et coll. Ramifications diagnostiques de l’occlusion vasculaire oculaire en tant que premier événement thrombotique associé au facteur V Leiden et à l’hétérozygotie du gène de la prothrombine. Clin Ophthalmol. 2015 Avril 3; 9: 591-600.
7. Purvin VA, Kawasaki A. Pièges Neuro-ophtalmiques courants., Cambridge, new york: Cambridge University Press, 2009.
8. Crawford C, Igboeli O. Un examen de l’inflammatoires chorioretinopathies: Le point blanc syndromes. ISRN l’Inflammation. 783190. .
9. Gass JD. Chevauchement entre le syndrome d’élargissement de l’angle mort idiopathique aigu et d’autres conditions. Arch Ophthalmol. 2001;119:1729-30.
10. Jampol LM, Tamisage PA, Pugh D, et al. Syndrome du point blanc évanescent multiple. I. Résultats cliniques. Arch Ophthalmol. 1984;102:671-4.
11. Jacobsen DM, Pomeranz HD. Maladies paranéoplasiques d’intérêt neuro-ophtalmique. Dans: Nj Newman, V Biousse, JB Kerrison, éd., Walsh et Hoyt de la Clinique de Neuro-Ophtalmologie, 6e ed. Volume 2. Philadelphie: Lippincott; 2005.
12. Parikh M, Miller NR, Lee AG, et coll. Prévalence d’une protéine C-réactive normale avec un taux de sédimentation érythrocytaire élevé dans l’artérite à cellules géantes éprouvée par biopsie. Ophthalmol. 2006 Oct;113 (10): 1842-5.
13. Barash P, Cullen B, Stoelting R, et coll. Anesthésie clinique, 6e édition, Section VII. Philadelphie: Lippincott, Williams et Wilkins; 2009.
14. Arnold AC. Pathogenèse de la neuropathie optique ischémique antérieure non artéritique. J Neuroophtalmol. 2003;23(2):157-163.
15., Collignon-Robe NJ, Feke GT, Rizzo JF. Circulation de la tête du nerf optique dans la neuropathie optique ischémique antérieure non artéritique et la névrite optique. Ophtalmologie. 2004;111(9):1663-72.
16. Fraunfelder FT, Roy FH. Thérapie Oculaire actuelle 2. Philadelphie: W. B Saunders; 1985.
17. Chevalier CL, Hoyt WF. Cécité monoculaire de drusen du disque optique. Am J Ophthalmol. 1972;73:890-4.
18. Sarac O, Tasci YY, Gurdal C, Can I. Différenciation de l’œdème du disque optique de la tête du nerf optique drusen avec la tomographie par cohérence optique du domaine spectral. J Neuroophtalmol. 2012 Sep;32 (3): 207-11.
19., Miller N, Subramanian P, Patel V. Walsh et Hoyt de la Clinique de Neuro-Ophtalmologie, l’essentiel, 3ème Ed. Wolters Kluwer; 2016.
20. Brosh K, Strassman I. Unilatérale de l’œdème papillaire dans pseudotumeur cérébrale. Semin Ophthalmol. 2013 Juillet; 28 (4): 242-3.
21. Ford CS, Biller J, Weaver RG. Défauts de champ associés à Drusen et hémorragies. Sud Med J. 1983; 6 (8): 1060-2.
22. van Endt JJ, Wessels HA. Élargissement de l’angle mort causé par un œdème papillaire. Am J Ophthalmol. 1988 Sept; 106 (3): 373.
23. Larner, AJ. Tous les maux de tête du matin ne sont pas dus à des tumeurs cérébrales. Pract Neurol. 2009 Avril; 9 (2): 80-4.
le 24., Rose GE. Obscurcissements visuels posturaux chez les patients atteints d’une maladie oculaire thyroïdienne inactive; une variante de la maladie” hydraulique ». Oeil (Lond). 2006 Oct;20 (10): 1178-85.
25. Comité de classification des Maux de tête de la Société Internationale des Maux de tête. La Classification Internationale des Troubles des Céphalées, 3e édition. Céphalalgie. 2013;33(9):629-808.