US Pharm. 2020;45(9):27-29.
resumen: desde que las hormonas sintéticas se combinaron por primera vez en la década de 1940, la terapia de reemplazo hormonal ha sido ampliamente utilizada por mujeres que experimentan síntomas menopáusicos indeseables. Las investigaciones posteriores llevaron a los descubrimientos de varios efectos negativos asociados con el uso de la terapia hormonal, lo que provocó discusiones sobre los riesgos frente a los beneficios del tratamiento hormonal., Debido a los riesgos asociados con las preparaciones comerciales, la terapia hormonal compuesta (CHT) se ha vuelto más prominente, ya que se ha promocionado como una alternativa biológicamente equivalente a las hormonas sintéticas. Sin embargo, debido a la supervisión mínima o nula de la FDA en el ámbito de los compuestos en general, CHT puede no ser tan seguro como se ha anunciado. En 2018, sobre la base de los resultados favorables de los ensayos, Bijuva se convirtió en la primera formulación de combinación bioidéntica 17-beta estradiol-progesterona aprobada por la FDA.,
durante décadas, las mujeres han recurrido a la terapia de reemplazo hormonal para tratar los síntomas vasomotores adversos asociados con la menopausia, como los sofocos y los sudores nocturnos. Las mujeres pueden pasar hasta un tercio de sus vidas en un estado de deficiencia hormonal, lo que contribuye aún más a efectos indeseables como cambios de humor, aumento del riesgo de osteoporosis y disminución de la libido. El estrógeno sistémico es el tratamiento más eficaz para los síntomas vasomotores, mientras que los síntomas genitourinarios asociados con la menopausia deben tratarse con una dosis baja de estrógeno tópico.,1 El estudio observacional de la salud de las mujeres en todo el país encontró que las mujeres experimentan síntomas vasomotores durante un promedio de 7.4 años después de la menopausia.2 Sin embargo, la mayoría de los médicos recomiendan que el tratamiento no dure más de 5 años después de la menopausia y recomiendan encarecidamente evitar la terapia hormonal por completo en mujeres mayores de 60 años.1 el médico debe sopesar cuidadosamente los riesgos y beneficios asociados con las hormonas sintéticas y compuestas, teniendo en cuenta el objetivo principal de mejorar la calidad de vida del paciente.,
hormonas bioidénticas
Las hormonas bioidénticas, como estrógenos, progestinas y andrógenos, son compuestos que se preparan de acuerdo con el capítulo de la USP<795 > normas de composición no esteril. Estas hormonas pueden ser compuestas en una variedad de dosis y formas de dosificación, creando muchas opciones para las mujeres interesadas en la terapia hormonal compuesta (CHT)., Las formulaciones compuestas no se someten a las estrictas pruebas de estándares de fabricación y pureza que hacen sus contrapartes aprobadas por la FDA; sin embargo, a pesar de este entorno no regulado, el CHT es ampliamente popular entre los pacientes que buscan medicamentos más «personalizados».
La Sociedad Endocrina ha definido las hormonas bioidénticas compuestas como » compuestos que tienen exactamente la misma estructura química y molecular que las hormonas que se producen en el cuerpo humano.,»3 la FDA afirma que el término hormona bioidéntica es puramente una estrategia de marketing, ya que no existe una base científica para un beneficio implícito o una reducción del riesgo para la CHT en comparación con la terapia hormonal sintética aprobada por la FDA.3
terapia hormonal sintética
la FDA aprobó el dietilestilbestrol en 1941 y los estrógenos equinos conjugados (CEE) en 1942 para tratar los síntomas menopáusicos.4 A partir de la década de 1960, las ventas de estrógeno se dispararon hasta 1975, cuando surgieron informes de que el uso de estrógeno podría estar asociado con un mayor riesgo de cáncer de endometrio.,4 Sin embargo, estos informes fueron ignorados en gran medida, y el uso de estrógeno continuó. No fue hasta 1996, cuando se publicó el ensayo Postmenopáusico de intervenciones de estrógeno/progestina (PEPI), que los proveedores de atención médica comenzaron a comprender realmente los posibles efectos negativos asociados con la terapia con estrógenos. PEPI fue un ensayo multicéntrico, doble ciego, aleatorizado, controlado con placebo, de 3 años de duración, que examinó los efectos histológicos endometriales de la terapia con estrógeno sintético sin oposición versus tres regímenes diferentes de estrógeno sintético más progestina.,5
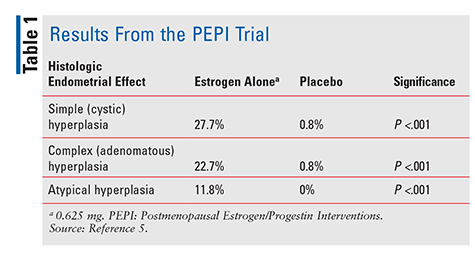
en el ensayo PEPI, significativamente más sujetos que recibieron estrógeno solo desarrollaron hiperplasia endometrial simple, compleja o atípica en comparación con los sujetos que recibieron placebo (tabla 1). Además, aunque no se especificaron los porcentajes exactos, las tasas de hiperplasia en los sujetos a los que se administró uno de los tres regímenes de estrógeno más progestina fueron similares a las de los sujetos a los que se administró placebo.5 en resumen, la administración de estrógeno solo en una dosis de 0.,625 mg por día condujo a un aumento significativo de la incidencia de hiperplasia endometrial, mientras que la combinación de EEC con progestina protegió el endometrio del crecimiento excesivo en un grado considerable.5 debido a este riesgo probado de cáncer de endometrio, la progestina siempre se administra en combinación con estrógeno en mujeres con un útero intacto. Para confirmar aún más este riesgo, una serie de casos de 2007 describió a tres mujeres que usaron CHT con dosis subterapéuticas de progestina y luego desarrollaron cáncer de endometrio.,6
El ensayo PEPI, junto con los resultados de 16,068 mujeres posmenopáusicas de la iniciativa de salud de la mujer (WHI) publicada en 2002, arrojó luz sobre las serias preocupaciones planteadas en la década de 1970.7 aunque el ensayo PEPI no mostró un mayor riesgo de hiperplasia con el producto combinado, el Whi encontró riesgos significativamente mayores asociados con el uso de hormonas sintéticas, como enfermedades cardiovasculares, accidentes cerebrovasculares, eventos tromboembólicos y cáncer de mama.,7 hubo un aumento del 80% del riesgo de enfermedad cardiovascular 1 año después de la interrupción de la terapia combinada CEE/acetato de medroxiprogesterona, y un aumento del 37% del riesgo de ictus isquémico durante la fase de intervención con la terapia combinada. Además, el riesgo de cáncer de mama aumentó significativamente (24%) durante la intervención. El uso de estrógeno más progestina sí proporcionó algunos beneficios, y las pacientes observaron una menor incidencia de atrofia vaginal, síntomas vasomotores reducidos, como sofocos y sudores nocturnos, y un 38% menos de riesgo de cáncer colorrectal durante el tratamiento con terapia combinada.,7 no obstante, debido a la importancia del aumento del riesgo de cáncer de mama y de episodios tromboembólicos, el ensayo se suspendió pronto.
terapia hormonal compuesta
Los riesgos discutidos anteriormente allanaron el camino para la defensa de la CHT porque se pensó que adaptar o personalizar la CHT al paciente individual maximizaría el beneficio y minimizaría el riesgo. Las afirmaciones de que el CHT era más seguro y biológicamente más amigable se hicieron más prominentes, y su uso aumentó., Pinkerton y Santoro utilizaron dos encuestas diferentes, Harris y Rose, para evaluar el conocimiento de los pacientes sobre la TCH y cuantificar el uso de la TCH en comparación con la terapia hormonal aprobada por la FDA, respectivamente.8 los resultados de la encuesta Harris indicaron que el 86% de las mujeres de 40 a 65 años desconocían que el CHT no estaba aprobado por la FDA, y los resultados extrapolados de la encuesta Rose sugirieron que, anualmente, hasta 2.5 millones de mujeres mayores de 40 años pueden usar CHT.8 los datos de ambas encuestas indicaron que un médico o farmacéutico había recomendado CHT., Estos resultados sugieren que existe una oportunidad para que los proveedores se aseguren de que los pacientes estén informados sobre el producto que están recibiendo, incluidos todos los posibles riesgos asociados con la terapia hormonal, y para que los farmacéuticos de compuestos se aseguren de que están suministrando un producto terapéuticamente puro en el que los pacientes puedan confiar.
debido a que la FDA no es responsable de la estandarización de productos compuestos, la regulación a menudo recae en las Juntas Estatales de farmacia., Estas juntas generalmente no tienen los recursos para llevar a cabo inspecciones regulares de Farmacias de compuestos, y la FDA interviene solo cuando se presenta una queja.9 aunque las formulaciones compuestas no están legalmente requeridas para llevar advertencias de riesgo, teóricamente estos productos pueden presentar los mismos riesgos que los mencionados anteriormente para la terapia hormonal sintética. Hasta la fecha, sin embargo, no ha habido ensayos de seguridad cabeza a cabeza de CHT versus hormonas sintéticas.,10
Hay tres tipos de estrógenos que una mujer puede recibir como parte de un régimen de reemplazo hormonal compuesto: estrona (E1), estradiol (E2) y estriol (E3), cada uno con un grado variable de potencia (E2 > E1 > E3).9 debido a que compiten por el mismo receptor, estos estrógenos actúan como inhibidores competitivos, lo que resulta en una disminución de la eficacia si no se equilibra correctamente.,11 En consecuencia, los defensores de la CHT desarrollaron Biest (E2 + E3 en una formulación de 20/80) y Triest (E1 + E2 + E3 en una formulación de 10/10/80) con el fin de maximizar la potencia fisiológica, pero actualmente no hay evidencia que apoye la afirmación de que estas formulaciones en estas proporciones confieran algún beneficio de seguridad en comparación con la terapia hormonal sintética.11
aunque en general el CHT no se ha estudiado adecuadamente y no se ha regulado, en octubre de 2018, según los hallazgos del ensayo REPLENISH, Bijuva se convirtió en la primera formulación de combinación bioidéntica 17-beta estradiol-progesterona aprobada por la FDA., REPLENISH, un estudio multicéntrico de fase III, aleatorizado, doble ciego, controlado con placebo, investigó la eficacia, la seguridad endometrial y la seguridad general de cuatro dosis diferentes de una sola cápsula de 17-beta estradiol-progesterona para síntomas vasomotores moderados a graves en mujeres posmenopáusicas.La variable principal de seguridad fue la incidencia de hiperplasia endometrial a los 12 meses. A los 12 meses, no se observaron casos de hiperplasia endometrial para ninguna de las formulaciones de dosis de estradiol-progesterona.,12 a las 12 semanas, la formulación de estradiol 1 mg–progesterona 100 mg demostró la mayor reducción estadísticamente significativa en la frecuencia y gravedad de los síntomas vasomotores en comparación con el placebo, manteniendo al mismo tiempo los estándares primarios de seguridad.12 Sin embargo, como se mencionó anteriormente, no ha habido ensayos que comparen la seguridad de las hormonas sintéticas versus las formulaciones de hormonas bioidénticas, por lo que teóricamente los riesgos permanecen.,
conclusión
según el ensayo REPLENISH, las mujeres pre, peri y posmenopáusicas ahora tienen un tratamiento estandarizado, regulado, bioidéntico y aprobado por la FDA para los síntomas vasomotores. Se necesitan ensayos futuros para delinear completamente el perfil de seguridad de 17-beta estradiol y CHT. Los farmacéuticos deben recomendar cualquier formulación hormonal oral durante el menor tiempo posible., Además, si se elige CHT, los farmacéuticos deben asegurarse de que sus pacientes sepan qué es CHT y en qué se diferencia de las hormonas sintéticas, al tiempo que mantienen una conversación franca sobre los beneficios y riesgos de la terapia de reemplazo hormonal.
1. Martin KA, Manson JE. Acercamiento al paciente con síntomas menopáusicos. J Clin Endocrinol Metab. 2008;93(12):4567-4575.
2. Avis NE, Crawford SL, Greendale G, et al. Duración de los síntomas vasomotores menopáusicos durante la transición de la menopausia. Jama Intern Med. 2015;175(4):531-539.3. Santoro N, Braunstein GD, Butts CL, et al., Compounded bioidentical hormones in endocrinology practice: an Endocrine Society scientific statement (en inglés). J Clin Endocrinol Metab. 2016;101(4):1318-1343.
4. Stefanick ML. Estrógenos y progestinas: antecedentes e historia, tendencias en el uso, y directrices y regímenes aprobados por la administración de alimentos y Medicamentos de los Estados Unidos. Am J Med. 2005; 118 (suppl 12B): 64-73.
5. Grupo de escritura para el juicio PEPI. Efectos de la terapia de reemplazo hormonal sobre la histología endometrial En mujeres posmenopáusicas. El ensayo posmenopáusico de intervenciones de estrógeno / progestina (PEPI). JAMA. 1996;275(5):370-375.
6., Eden JA, Hacker NF, Fortune M. tres casos de cáncer de endometrio asociados con la terapia de reemplazo hormonal «bioidéntica». Med J Aust. 2007;187(4):244-245.
7. Rossouw JE, Anderson GL, Prentice RL, et al. Riesgos y beneficios del estrógeno más progestina en mujeres posmenopáusicas sanas: principales resultados del ensayo controlado aleatorizado Women’s Health Initiative. JAMA. 2002;288(3):321-333.
8. Pinkerton JV, Santoro N. Compounded bioidentical hormone therapy: identifying use trends and knowledge gaps among US women. Menopausia. 2015;22(9):926-936.
9. Bhavnani BR, Stanczyk FZ., Concepto erróneo y preocupaciones sobre las hormonas bioidénticas utilizadas para la terapia hormonal compuesta personalizada. J Clin Endocrinol Metab. 2012;97(3):756-759.10. Prospecto de Bijuva (estradiol y progesterona). Boca Raton, FL: TherapeuticsMD, Inc; Noviembre 2019.11. Kuhl H. farmacología de estrógenos y progestágenos: influencia de diferentes vías de administración. Climatérico. 2005; 8 (suppl 1): 3-63.12. Lobo RA, Archer DF, Kagan R, et al. A 17beta-estradiol-progesterona oral capsule for vasomotor symptoms in postmenopausal women: a randomized controlled trial. Obstet Gynecol., 2018;132(1):161-170.
el contenido de este artículo es solo para fines informativos. El contenido no pretende ser un sustituto del asesoramiento profesional. La confianza en cualquier información proporcionada en este artículo es únicamente bajo su propio riesgo.